产品中心
技术交流

扫描二维码
Takara高通量单细胞分选系统——助力心血管疾病研究
单细胞测序技术从出现开始,就一直受到高度的关注。不同于以往的“概念炒作”,单细胞测序技术帮助研究人员解决了很多重要的技术问题,在众多研究领域得到广泛的应用。作为人体最小的结构和功能单位,细胞虽小,却蕴含天地。跨越组织细胞间异质性的障碍、解析稀有细胞的内涵和秘密,单细胞测序正在不断带给我们新的发现。
高通量单细胞分选技术的出现,让单细胞测序技术驶入了高速快车道。研究人员可以更加高效地完成单细胞测序研究。各类单细胞图谱计划也相继出现,单细胞测序研究再上一个台阶。
今天要为大家介绍的这款Takara高通量单细胞分选系统,集分选、文库构建于一身,不同于以往的液滴包裹式分选系统,可以帮助您实现高标准、严要求的单细胞测序研究。它就是:
ICELL8® cx Single Cell System

ICELL8 cx系统通过纳升级液体分注的方式,将细胞悬液样品分注到系统专用的纳升体积微孔芯片中,实现单细胞的捕获分选。
液体分注

喷嘴孔径高达125 μm,游刃有余面对更多细胞类型分选。
分注过细胞悬液的微孔芯片会在ICELL8 cx系统的荧光成像模块下,接受严格的扫描检测。微孔芯片上5,184个微孔的扫描结果通过系统配备的CellSelect®软件分析判断,成功捕获到活单细胞的微孔会被标记。
芯片扫描

CellSelect®软件界面
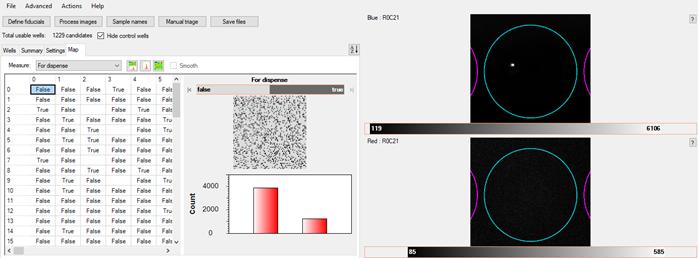
后续通过ICELL8 cx系统的液体分注模块,可以向被标记的微孔中加入文库构建所需的各种试剂。如,构建单细胞RNA-Seq文库需要的反转录反应试剂、各种需要的index接头等。您有想法,ICELL8 cx助您实现。
客户案例
中国医学科学院阜外医院心血管疾病国家重点实验室王利教授团队,针对动脉粥样硬化患者病变动脉组织中的血管平滑肌细胞(VSMC)进行了研究。该团队使用了Takara ICELL8单细胞分选平台完成了血管平滑肌细胞分选及单细胞测序文库构建实验。通过对血管平滑肌细胞的单细胞转录组分析鉴定到了维持VSMC特性的新关键调控因子——组蛋白变体H2A.Z。研究结果发表于《Circulation》上:Histone Variant H2A.Z is Required for the Maintenance of Smooth Muscle Cell Identity as Revealed by Single-Cell Transcriptomics。
单细胞分选示意图

目前,ICELL8 cx系统已经适配了多种即用型试剂,包括:
▪ 3’Differential Expression
▪ Human TCR a/b Profiling
▪ 5’Differential Expression
▪ SMART-Seq Full-length Transcriptome Analysis
基于上一代Takara单细胞分选系统ICELL8,一些仪器使用者成功开展了多种应用类型的高通量单细胞测序,如,ATAC-Seq、CUT & Tag-Seq。
高通量单细胞测序研究还有更多可能,ICELL8 cx Single Cell System将持续给您带来更多惊喜。
如果您还在使用孔板,Takara单细胞分选平台为您的研究提速升级!
【参考文献】
Yao F, Yu P, Li Y, et al. Histone Variant H2A.Z is Required for the Maintenance of Smooth Muscle Cell Identity as Revealed by Single-Cell Transcriptomics[J]. Circulation, 2018, 138(20): 2274-2288
Wang L, Yu P, Zhou B, et al. Single-cell reconstruction of the adult human heart during heart failure and recovery reveals the cellular landscape underlying cardiac function[J]. Nature Cell Biology, 2020, 22(1): 108-119
Mezger, A. et al. High-throughput chromatin accessibility profiling at single-cell resolution[J]. Nature Communications, 2018, 9(1), 3647
Kaya-Okur H S, Wu S J, Codomo C A, et al. CUT&Tag for efficient epigenomic profiling of small samples and single cells[J]. Nature Communications, 2019, 10(1)