产品中心
技术交流

扫描二维码
自体来源干细胞和异体来源干细胞,该如何选择?
原创:硬核小蜜锋 文章来源:干细胞之父
在医疗手术中,移植自己的细胞或组织,往往意味着安全高效,但凡事并不绝对。比如间充质干细胞疗法,使用“自体”与“异体”就各有优势,选择也因人而异。通常而言,年龄与身体状况是重要的参考指标,一般40岁以上,或身体伴有疾病与亚健康状态时,不建议使用自体干细胞,反之可选。为什么会有这样的结论?本篇文章就将结合过往研究,与您详细探讨异体与自体干细胞之间的选择问题。
毫无疑问,间充质干细胞(MSC)是疾病治疗领域冉冉升起的一颗新星。
2022年,《Signal Transduction and Targeted Therapy》(影响因子:40.8)一项综述[1]称MSC是治疗神经系统疾病、呼吸系统疾病和肺纤维化、代谢/内分泌相关疾病、骨关节炎和心血管疾病的“潜力股”[1]。而在全球范围内,以干细胞对抗衰老也已经成为一种趋势,一种风尚。
△《Signal Transduction and Targeted Therapy》是《Nature》旗下的新期刊
不过谈到具体应用时,人们却分成了两派——有人偏向使用自体MSC,坚称:“自产自用”更安全,回输的干细胞更不容易被机体代谢。而“异体派”则认为:使用婴儿围产组织来源的异体MSC是在“变废为宝”,不但绕过了繁琐的采集,还获取了生物学特性更优异的MSC。
事实上,两者提到的观点都具有一定的道理。只是生活总存在各类变量,比如年龄、身体状况,使用时效,患者承受能力等等,它们会影响干细胞的使用,也会将这个问题引向不同的答案。
01
衰老与疾病
自体干细胞的两道“枷锁”
间充质干细胞(MSC),是自然组织修复再生系统的基础之一。凭借着强大的自我更新和多向分化能力,它能向成骨细胞、成肌细胞、脂肪细胞、软骨细胞等成基质谱系细胞分化。而除了出色的“可塑性”之外,MSC还具有免疫调节和抗炎的特性。
更难得的是,它的来源很广泛,在成年人的牙髓、脂肪、骨髓中都能发现它的身影。
这意味着,我们能从自己的身体里获得“良药”,并以自然的方式去“纠正”机体的疾病,修复内里的损伤,既没有伦理风险,也几乎不存在副作用。
这些优秀的特性吸引了大批的科学家,他们陆续将自体干细胞应用于治疗糖尿病、心脑血管疾病、神经退行性疾病等等疑难杂症,并颇有建树,自体干细胞也被陆续写入心力衰竭、下肢慢性缺血性疾病等疾病的专家共识里。
然而,在干细胞研究这股浪潮之中,研究者们也发现了自体干细胞的局限。
自体干细胞受限于年龄
我们体内的干细胞并不是一层不变的,其数量及功能都会随着年龄的增长而出现“断崖式”的滑坡。这种耗竭用数字图形表现起来非常直观,让我们逐一来看。
1、数量骤降95%
2007年,间充质干细胞之父Arnold Caplan测定了从出生到80岁的骨髓间充质干细胞(BM-MSC)的含量[2]。
在新生儿期,人体骨髓MSC含量最高,每1万个骨髓细胞里有1个是BM-MSC;而到了80岁,每200万个骨髓细胞里只能挑出1个BM-MSC。换句话说,80岁老人的骨髓MSC含量仅有新生儿的两百分之一,这也是为什么老年人骨折恢复特别缓慢的重要原因。
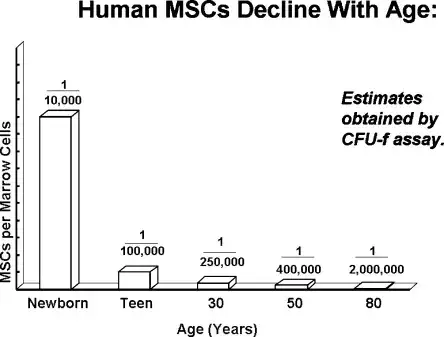
△人类骨髓中间充质干细胞含量随年龄变化图
2、扩增能力显著下降
强大的扩增能力是产生足量干细胞,满足临床治疗需求的基础,此前,亚利桑那大学医学院曾将参与者按照年龄分组,分别检测了来自年轻组(<30岁),成年组(35-50岁)和老年组(>60岁)脂肪间充质干细胞(AT-MSC)的扩增能力[3]。
他们发现,对比40岁以下的AT-MSC,50岁以上的AT-MSC表现出明显的衰老特征,如:SA-β-gal活性是鉴定衰老细胞最常用的生物标志物,而后者的含量几乎是前者的两倍多。
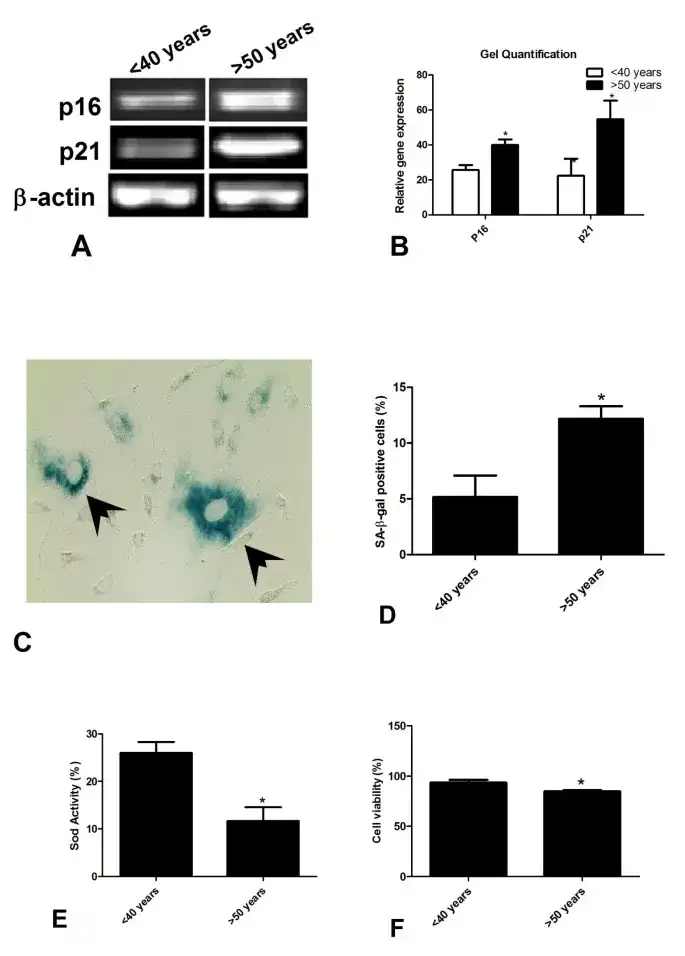
△从年轻和老年供体分离的AT-MSC中年龄相关参数的比较
在随后的扩增测试中,年轻组和成年组的干细胞也不出所料地扩增出更大的细胞集落,相较而言,老年组的细胞增殖速度更慢,细胞倍增时间显著增加,最后生成的集落也很小。
3、分化能力显著下降
亚利桑那大学医学院还就不同年龄段MSC的分化能力做了进一步分析,具体评估AT-MSC向脂肪细胞、骨细胞、软骨细胞及神经细胞分化的能力。其中成脂的分化潜能与年龄无关,但在比较后三者时,老年干细胞的“颓势”再次浮现。
向成骨细胞分化时:年轻组比成年组与老年组产生了更多的基质。同时RT-PCR分析显示,年轻的AT-MSC中成骨特异性基因的表达更高,以及骨钙素和碱性磷酸酶倍数表达。
向软骨细胞分化时:老年组在软骨基质形成和软骨相关基因表达方面显著落后,比如在聚集蛋白聚糖的表达上,年轻组:10.0 ± 1.5;成年组:4.3 ± 0.2;老年组:1.8 ± 0.4。综合结果表明:供体年龄负向调节AT-MSC向软骨分化。
向神经细胞分化时:无论供体年龄如何,AT-MSC都表现出神经元样分化,具有突出和细长的神经元结构,然而其他研究表明:在后期传代诱导AT-MSC扩增时,年轻的AT-MSC细胞还是优于老年细胞。
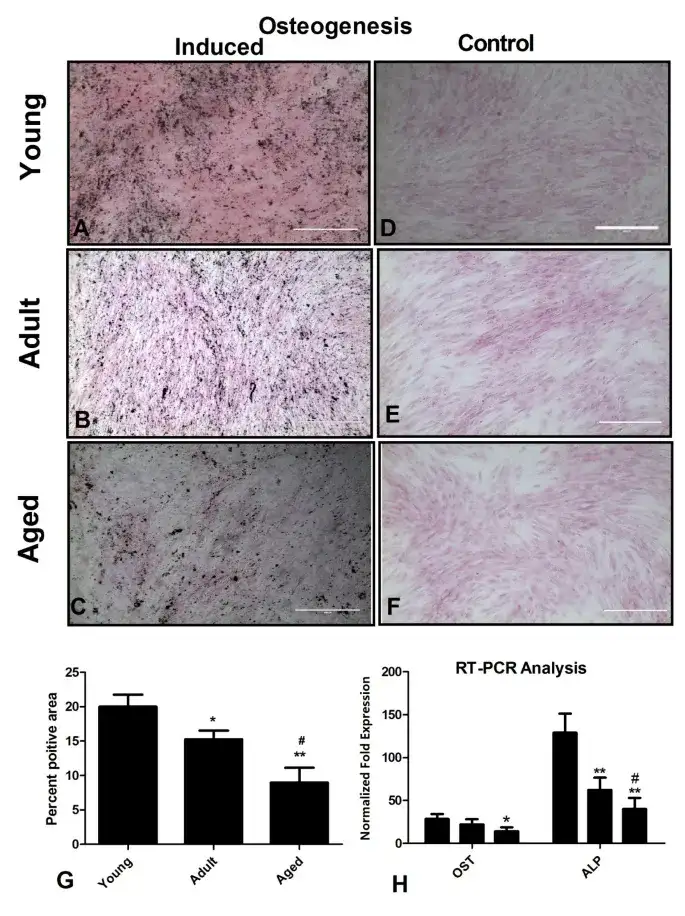
△供体年龄对 AT-MSCs 成骨潜力的影响
以上研究不难看出,年龄就像是干细胞质量的一道道门槛,随着岁月渐长,体内干细胞数量、及其扩增和分化能力都会有不同程度的下滑,甚至腰斩。而这种改变势必会影响到干细胞治疗的效果。
自体干细胞受限于供体健康
除了年龄之外,一些疾病的存在也会“重创”体内的干细胞。
2017年,《Stem Cells Translational Medicine》(影响因子:6.9)上有一则研究就证实[4]:长期患有2型糖尿病会降低干细胞的增殖能力、免疫抑制潜力及存活率。文章明确建议:当病患患有糖尿病超过10年且较为肥胖时,不再适合使用自体干细胞进行治疗。
除此以外,有文章还称从系统性红斑狼疮、类风湿关节炎和特发性血小板减少性紫癜患者骨髓中分离出的MSC存在异常形态,并伴有增殖速度减慢、和免疫调节功能下降的态势。
所以综合来看,如果你年纪不超过40岁,且身体健康(没有影响干细胞质量的疾病或亚健康状态),那么自体间充质干细胞会是一个很好的选择,除此之外,则建议选择异体间充质干细胞。
02
“异”军突起
异体干细胞打开成药可能性
听到异体,许多人第一反应是要配型,这里我们要明晰一个概念:与造血干细胞不同,回输异体MSC是不需要配型的,因为MSC的免疫原性很低——不表达白细胞抗原HLA-DR,且仅表达可以忽略的HLA-A、HLA-B,因此,即使异体使用也不会触发免疫排斥反应。
这道“豁免金牌”极大地拓宽了异体MSC的使用范围,也让自体与异体研究的数量走势总体相当,而到近些年,异体MSC研究甚至隐隐有超越之势。
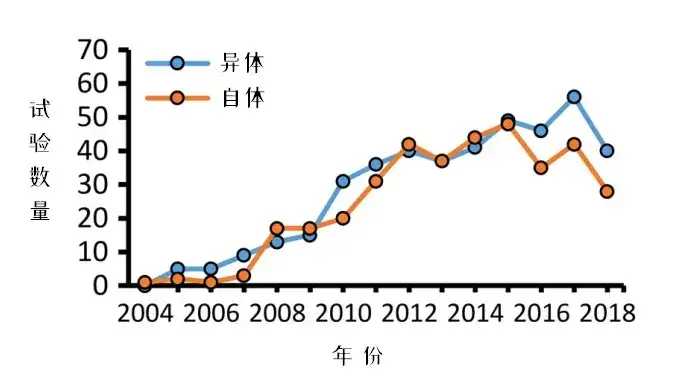
△2004-2018年间充质干细胞临床试验趋势
为什么会这样?这其实是多因素造成的结果。
首先,异体MSC多源自于婴儿的围产组织,如胎盘、脐带和羊膜等,这类MSC素有“零岁细胞”之称,生来没有“年龄焦虑”。
2021年,爱尔兰国立大学曾对比脐带间充质干细胞(UC-MSC)、脂肪间充质干细胞(AT-MSC)和骨髓间充质干细胞(BM-MSC)之间的生物学特性[5],他们发现:
1、论增殖能力:UC-MSC>AT-MSC>BM-MSC;
2、论免疫原性:UC-MSC的HLA抗原表达最低,并不容易被免疫系统清除;
3、论免疫调节:UC-MSC>AT-MSC和BM-MSC;
4、论抑制炎症:UC-MSC、BM-MSC和AT-MSC都能有效抗炎,只是机制略有不同;
5、论分化潜能:存在一种由表观遗传因素驱动的“组织记忆”效应,驱使BM-MSC易分化为成骨细胞和软骨细胞,AT-MSC易分化为脂肪,UC-MSC则比较特殊,它在分化为成骨细胞及软骨细胞上能压过BM-MSC,并具有相对较高的胰腺再生和神经再生潜力。

△ UC-MSC、AT-MSC及BM-MSC生物差异性对比,图中额外增加表面标志物对比
所以对比其他组织来源的MSC,UC-MSC应该是临床中泛用性更强,生物学特性更优异的间充质干细胞。
其次,在生物学特性之外,异体MSC比自体MSC更具有时效性。作为“一对一”的定制化治疗,自体MSC治疗要经历多个步骤:从患者体内采集干细胞——在实验室培养(约4周)——进行治疗等步骤,这通常需要耗费一个月以上,对于需求迫切的急性疾病(如脊髓损伤、心肌梗塞等)而言,这是“致命”的缺陷。
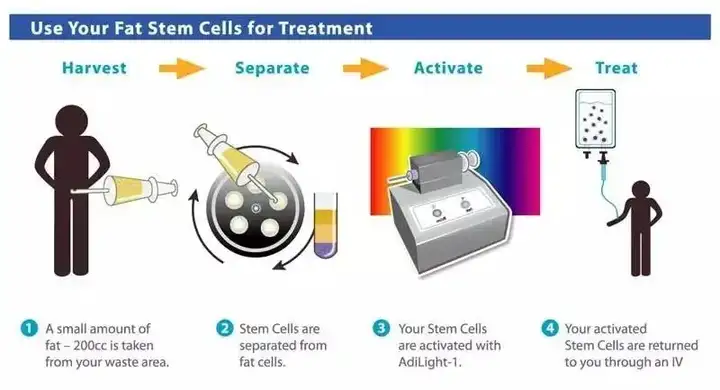
△ 图片为自体脂肪干细胞制备的过程,每个病患都将是一个独立的生产线
相较而言,异体MSC所有的生产流程都可以发生在“有需求”前,生产药企会提前从健康供体身上提取MSC,通过分离,扩增等步骤将其制备成药,而后,这些药品会被放置于仓库冻存,静待“随取随用”,因此,异体MSC是真正有望实现批量化、规范化生产的“细胞药品”。
最后与采集繁琐程度有关,自体干细胞的采集通常使用“骨髓穿刺”和“抽脂手术”,我们以程度较轻的抽脂举例,手术时,医生会将一根空心金属管(直径从1mm到10mm不等)伸入患者的皮下脂肪层,一边“捣烂”脂肪,一边连血带脂地抽出脂肪组织。这番景象常常会“劝退”患者,而异体MSC直接省略掉了这一步骤。
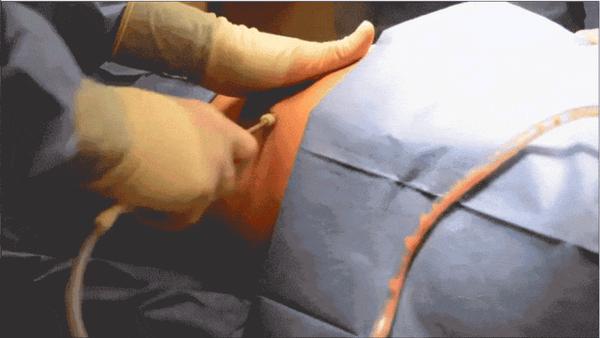
△ 抽脂其实也是一种需要麻醉的外科手术
不用配型,较好生物学特性及便捷高效的使用,这些优势打开了异体干细胞成药及治疗更多疾病的可能性,也让其成为了目前干细胞治疗的有力选择。
总的来说,在能保障细胞质量的前提下,无论异体MSC还是自体MSC都能给予患者非凡的益处。但基于每个人不同的情况,40岁以下,且身体健康可选自体MSC ;40岁以上,或身体存在疾病或亚健康状态可选异体MSC。
03
集优点于一身
iPS技术开创治疗新路
而随着再生医学的发展,我们或许不再需要于自体与异体当中“择优而选”,一个同时具备“自取自用”及“优异生物学特性”的选项开始浮现,它就是诱导多能干细胞(iPSC)。
21世纪初,日本京都大学教授山中伸弥通过四个转录因子(OCT4、SOX2、KLF4和c-MYC),抹去了成熟纤维细胞的发育痕迹,使其退回到类似胚胎干细胞(ESC)的状态,即iPSC。
iPSC拥有不输ESC的“全能分化性”,能在适当的诱导下分化为动物体内几乎所有细胞类型,比如心肌细胞、胰岛细胞与神经细胞,当然也包括本文的主角——间充质干细胞(iPSC-MSC)。
这极大地拓宽间充质干细胞的来源,它意味着,我们可以无视供体的年龄与身体状况,只需用iPS技术将供体细胞转变为iPSC,并进一步诱导,就可以得到具有年轻遗传特征的iPSC-MSC。
与天然的MSC相比,iPSC-MSC的具有诸多优势,据国际期刊《Stem Cell Research & Therapy》今年10月发表的一篇论文[6]表示:
1、iPSC-MSC具有更强的增殖能力,并减少了与年龄相关的变化和异质性。
2、分化能力方面,iPSC-MSC的脂肪分化能力较强;在免疫相关功能方面,iPSC-MSC表现出更强的免疫抑制能力。与UC-MSC相比,iPSC-MSC的抗炎因子表达更高,这使得它们在治疗免疫相关疾病中更具潜力。

△ 论文:诱导多能干细胞来源的间充质干细胞:能否成为细胞治疗的新星
这种优势也延续到了疾病治疗里面。研究者发现:iPSC-MSC所展现的功能与传统MSC类似,同样具有调节免疫反应和促进组织修复,也同样在治疗缺血和炎症相关病症——如心肌梗死、下肢缺血、炎症性肠病和急性肺损伤等疾病上展现出不俗的潜力。而得益于突出的性质,iPSC-MSC在骨关节炎、椎间盘退变等研究中的治疗效果要优于传统MSC。
丰富的来源、充足的数量、良好的治疗效果、高度同质性、还有能够有效解决免疫排斥及伦理问题,iPSC-MSC就像一个集“自体”与“异体”优势于一体,且生物学特性还要更上一层楼的“最佳选项”,被科学家们视作未来细胞疗法的关键细胞来源,也引领着干细胞新的治疗方向。
参考资料:
[1]Stem cell-based therapy for human diseases.https://doi.org/10.1038/s41392-022-01134-4
[2]Adult mesenchymal stem cells for tissue engineering versus regenerative medicine.https://doi.org/10.1002/jcp.21200.
[3]Donor age negatively impacts adipose tissue-derived mesenchymal stem cell expansion and differentiation.https://doi.org/10.1186/1479-5876-12-8
[4]Type 2 diabetes mellitus duration and obesity alter the efficacy of autologously transplanted bone marrow-derived mesenchymal stem/stromal cells.https://doi.org/10.1002/sctm.20-0506
[5]When Origin Matters: Properties of Mesenchymal Stromal Cells From Different Sources for Clinical Translation in Kidney Disease. https://doi.org/10.3389/fmed.2021.728496
[6]Induced pluripotent stem cell-derived mesenchymal stem cells: whether they can become new stars of cell therapy. https://doi.org/10.1186/s13287-024-03968-x
内容来源华夏源干细胞,旨在科普相关知识,传递行业前沿进展,不作为医疗指导建议,如需就医请到正规医院就诊。
【关于逐典】
上海逐典生物科技有限公司,坐落于中国(上海)自由贸易试验区,获得ISO9001质量体系认证,是一家从事重组蛋白研发和销售的高新科技企业。
逐典生物始终秉持以客户为中心的理念,针对重组蛋白的结构设计、纯化工艺及其稳定剂型相关的多项关键技术进行优化。专业定向蛋白变复性技术,可将大肠杆菌大量表达的变性固体蛋白转变成高活性可溶性蛋白。凭借技术优势,逐典生物新品研发周期短且可控性强,为重组蛋白的高质高效研发提供保障,为企业生产降本增效。
公司自成立以来成功开发百余种高活性细胞因子及多种高活性蛋白酶,覆盖细胞培养、病毒纯化以及质量分析等生物工艺各个环节。可广泛应用于科研、医药生产及IVD(体外诊断试剂)等领域,满足各类用户所需。
