产品中心
技术交流

扫描二维码
不会缺席的TCE双抗
文章原创: 东风 文章来源:药闻窗
T细胞衔接器(T Cell Engager,TCE)双抗指的是一种能同时结合肿瘤相关抗原(TAA)和T细胞上CD3的双特异性抗体。设计目的是希望将T细胞定向到肿瘤细胞,从而使T细胞能有效地杀伤肿瘤细胞。
目前来看,TCE通过借助T细胞来实现肿瘤杀伤作用,已在血液瘤中实现突破。例如,在血液肿瘤中,CD3搭配CD19、CD20和BCMA等靶点均已有药物上市,效果突出。在此基础上,TCE类药物在向实体瘤和自免适应症中迈进。在实体瘤中,Amgen创新药物Tarlatamab(CD3/DLL3)已在美国实现上市销售,CD3/CLDN18.2、CD3/EGFR和CD3/PSMA等药物均在临床早期展现良好效果。在自免适应症中,安进的CD3/CD19双抗Blinatumomab在6个难治性类风湿关节炎(RA)患者的初步数据中显示出积极疗效。
01
TCE双抗是什么?
双特异性抗体由于含有两种抗体的特异性,可以结合同一种抗原的两种表位或两种不同抗原的表位。双特异性抗体通过效应位点和靶点位点发挥其功能特性。效应位点起到连接募集效应细胞、药物分子或病毒的作用;靶点位点可以靶向到分子或细胞等。T细胞双特异性抗体是可以将T细胞与肿瘤细胞连接的治疗性抗体。
大多数TCE有三个结构域:一个结构域与T细胞受体的组分结合,一个结构域与肿瘤相关抗原结合,第三个结构域提供额外的功能,如延长半衰期。与常规的IgG相比,TCE被认为比Fc介导的ADCC更有效。与抗体药物偶联物(antibody drug conjugates,ADC) 相比,TCE的细胞毒性依赖于宿主的免疫系统,而不是化学有效载荷的细胞毒性,它攻击休眠状态和积极分裂的癌细胞,安全性更好。
TCE双抗,尤其是靶向CD3+T细胞重定向双特异性抗体,成为近年来双特异性抗体的研究热点。
02
CD3在TCE中的核心地位
T细胞表面存在众多CD分子,如CD3、CD4、CD8、 CD28等,CD3分子是众多分子中最为关键的T细胞表面分子。
(1)CD3是T细胞受体(TCR)的重要辅助蛋白,与TCR一同产生下游信号
【1】TCR接受来自MHC分子递送的抗原,并产生下游信号。TCR可接受来自MHC I类或MHC II类分子的抗原,并将细胞外信号转导到细胞内部,从而产生下游信号传导。
【2】TCR受体蛋白因为细胞内氨基酸过短,因此需要CD3来辅助传导信号。TCR受体蛋白绝大部分位于细胞外,胞内基本只有3个氨基酸左右的长度,因此在传导胞外信号到胞内时,需要CD3蛋白来辅助TCR受体蛋白来进行信号传导。
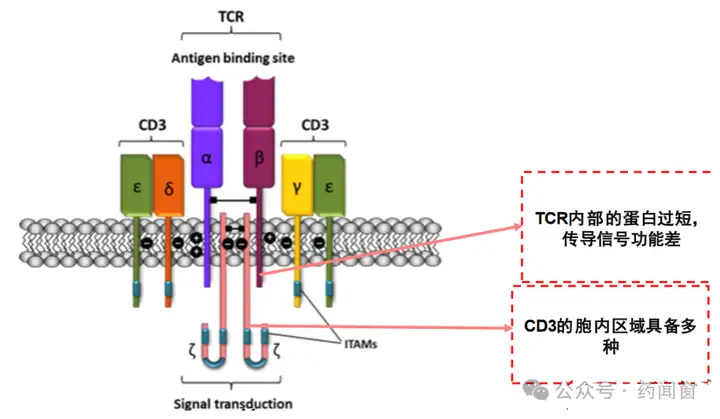
图1 CD3辅助传导信号优势
(2)CD3是T细胞重要标志物,具备多种功能,靶点成药性好CD3分子是T细胞膜上的重要生物标志物,包括四条蛋白质链(CD3γ,CD3δ,CD3ε和CD3ζ),其中两对异二聚体(CD3γε和CD3δε)是由CD3γ、CD3δ和CD3ε亚基的细胞外结构域组合而成的。异二聚体和T细胞受体共同形成TCR/CD3复合物,参与T细胞抗原识别、信号转导和T细胞发育的调控。
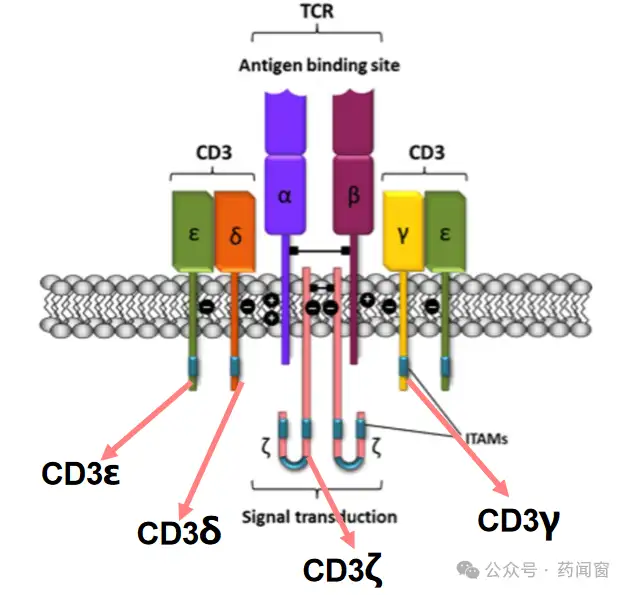
图2 CD3的结构
截止2022年,针对CD3分子获批的抗体药物数量排名第二,仅次于PD-1类抗体药物。
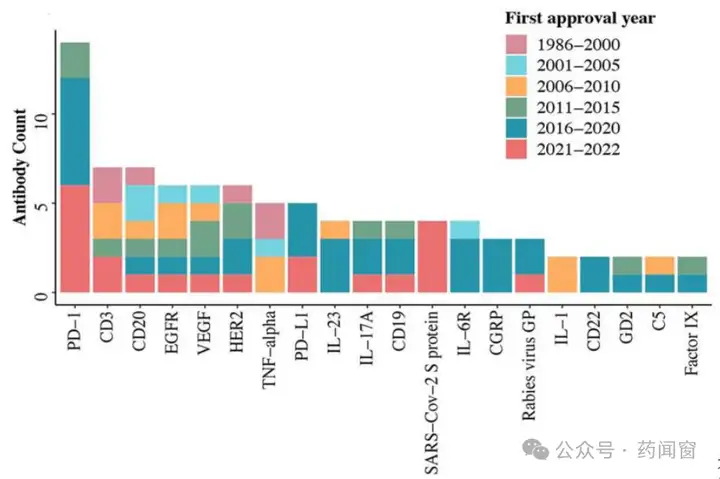
图3 不同靶点获批的抗体药物
(3)机制特殊,CD3类药物多以多抗形式存在
传统类肿瘤抗体药物主要以TAA(tumor-associated antigen)为主,TAA是在肿瘤细胞上高表达,但在健康细胞上表达水平较低。
传统的肿瘤抗体药物主要以TAA来进行设计,如HER2、EGFR和CD20等,该机制设计的抗体主要通过CDC、ADCC等功能来对肿瘤细胞进行特异性杀伤,从而抑制肿瘤生长。
CD3通过借助T细胞来进行杀伤肿瘤,并非传统TAA。CD3类药物多以多抗形式存在,主要以CD3搭配TAA的形式来进行设计。TAA端的设计目的在于帮助抗体靶向肿瘤组织,而CD3端能靶向T细胞,通过借助T细胞释放的肿瘤杀伤物质(穿孔素/颗粒酶等)来进行抑制肿瘤。
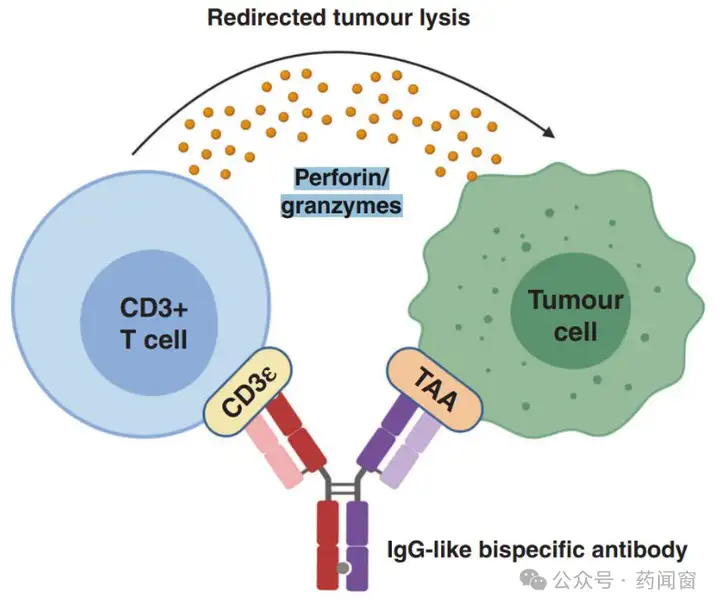
图4 CD3/TAA类抗体杀伤肿瘤的机制
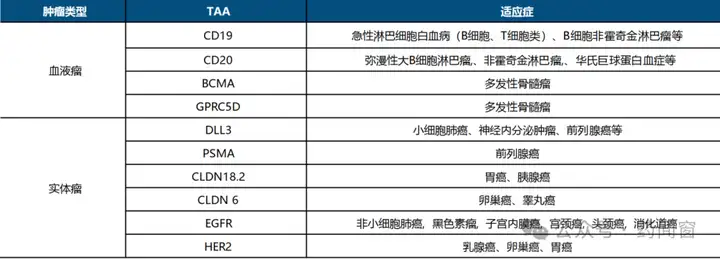
CD3搭配TAA来进行肿瘤靶向,不同的TAA选择让CD3类药物针对不同肿瘤。
表1 CD3/TAA针对肿瘤类型
03
CD3双抗CD3/CD20双抗
CD3/CD20双抗是一种创新性肿瘤治疗疗法。CD20是一种位于B细胞表面的非糖基化跨膜磷蛋白,主要在前B细胞到成熟B细胞阶段表达,其广泛存在于正常B细胞以及B细胞来源的淋巴瘤、白血病等的肿瘤细胞中。同时靶向B细胞来源的肿瘤细胞表面CD20抗原与免疫T细胞表面的CD3抗原,将T细胞募集至肿瘤处并激活其杀伤作用,为非霍奇金淋巴瘤(NHL)等血液肿瘤提供新治疗策略。
目前共有3款CD3/CD20双抗获批上市。艾伯维的Epcoritamab获批用于治疗复发性/难治性(R/R)弥漫大B细胞淋巴瘤(DLBCL)及滤泡性淋巴瘤(FL)患者,罗氏的Glofitamab获批治疗R/R-DLBCL患者,而罗氏的Mosunetuzumab则获批治疗R/R-FL患者。
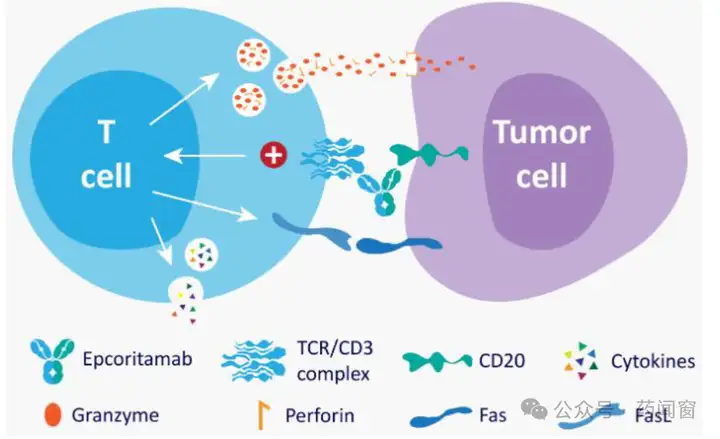
图5 CD3/CD20作用机制(以Epcoritamab为例)
Epcoritamab疗效与安全性俱佳。在已上市的四款CD3/CD20双抗中,Epcoritamab在R/R DLBCL与R/R FL两项适应症中均展现卓越疗效与良好安全性,其2023年销售额已到达3100万美元。
表2 CD3/CD20双抗上市产品数据对比
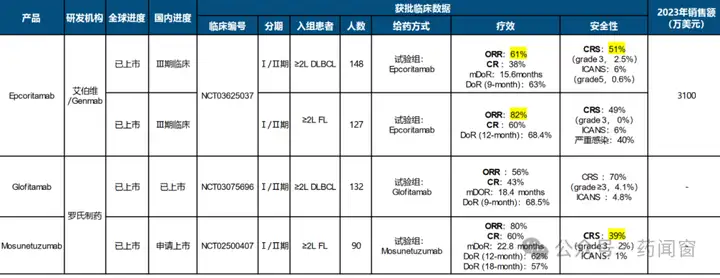
表3 CD3/CD20双抗研究进展
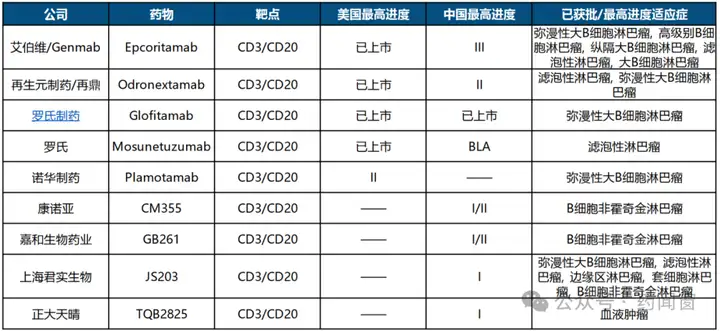
CD3/CD19双抗
CD19是一种95kDa的跨膜糖蛋白,作为免疫球蛋白超家族的一员,它在B细胞发育的各个阶段均有表达(除浆细胞外)。CD19高表达于大多数急性淋巴细胞白血病(ALL)、慢性淋巴细胞白血病(CLL)和B细胞淋巴瘤而在其他多数B细胞恶性肿瘤中表达较低。在前体B细胞ALL(BCP-ALL)中,CD19表达率接近100%。
目前仅1款CD3/CD19双抗获批上市。目前上市的靶向CD19的双抗药物数量有限,安进的Blinatumomab是全球获批的首个也是唯一一个CD3/CD19双抗,其被FDA批准用于治疗成人和儿童R/R BCP-ALL患者以及成人和儿童第一次或第二次完全缓解后,微小残留病(MRD)大于或等于0.1%的BCP-ALL患者。在中国,Blinatumomab获批用于治疗成人和儿童R/R BCP-ALL。
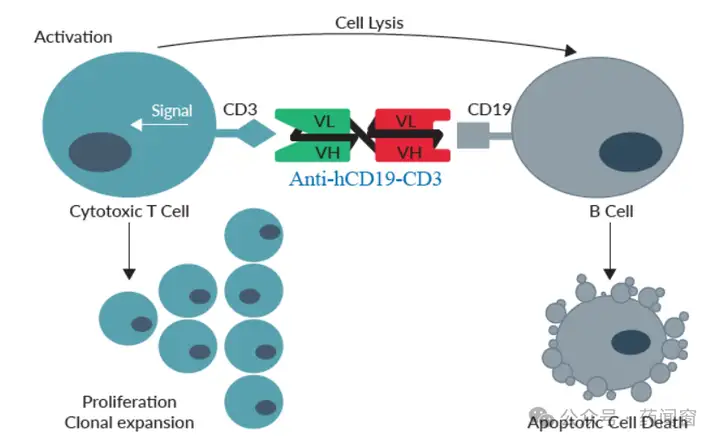
图6 CD3/CD19作用机制
CD3/CD19双抗Blinatumomab上市后全球销售额展现出持续增长态势,2021年至2023年销售额分别为4.72亿美元、5.83亿美元和8.61亿美元。2023年的高增长主要来自于临床中对该产品在B-ALL中的认知逐渐加深。
表4 Blinatumomab主要获批临床数据
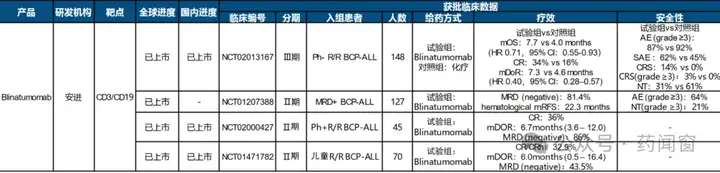
表5 CD3/CD19双抗研究进展
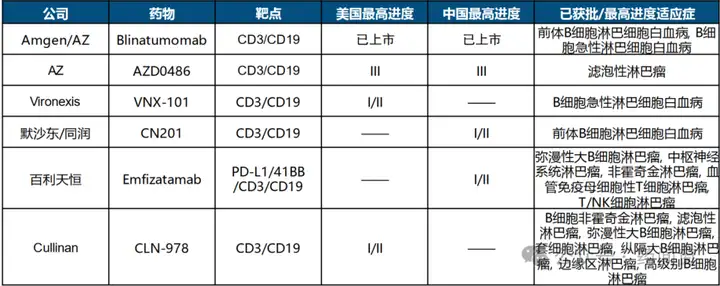
MSD与同润生物就CN201达成高达13亿美元交易。2024年8月9日,默沙东(MSD)宣布与同润生物达成协议,默沙东通过7亿美元的首付款和最高6亿美元的里程碑付款获得CN201的全球权益。CN201目前正处于1期和1b/2期临床试验的评估,分别用于治疗复发或难治性非霍奇金淋巴瘤(NHL)和复发或难治性B细胞急性淋巴细胞白血病(ALL)。
相较Blinatumomab更具便捷性。CN201通过结构优化(增加了Fc段),延长了药物的半衰期。Blinatumomab需24h持续静脉输注,共28天,而CN201输注方法为每周一次,每次持续2-3h左右,在治疗便捷性方面得到了明显的提升。
CN201早期临床试验结果积极。CN201治疗成人R/R B-ALL的I期研究结果显示,在目标剂量达到20mg以上的剂量组,ORR达70%以上,且获得缓解的患者中90%以上为MRD阴性。安全性方面,总体CRS发生率不到30%,3级CRS发生率为3.9%,目前总共入组51例成人患者,尚未出现ICANS(免疫效应细胞相关神经毒性综合征),总体安全性良好。
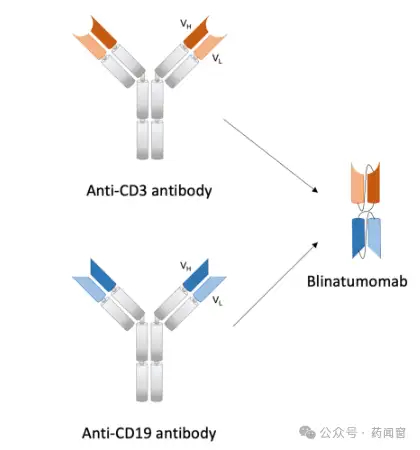
图7 Blinatumomab双抗结构
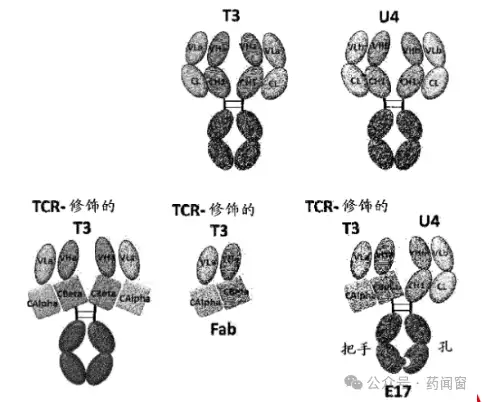
图8 CN201双抗结构
CD3/BCMA双抗
B细胞成熟抗原(BCMA)又称TNFRSF17,主要表达于成熟B淋巴细胞及浆细胞表面,其在多数MM细胞表面高表达,而在其他组织细胞中几乎不表达。BCMA通过介导下游信号通路,对MM细胞的存活、增殖、转移和耐药中起着关键性的作用,被视为治疗MM的极具潜力的抗原靶点。BCMA/CD3双特异性抗体通过同时结合T细胞上的CD3受体与MM细胞表面高表达的BCMA,激活并重定向细胞毒性T淋巴细胞(CTL)至肿瘤细胞处以介导其死亡。
已有2款CD3/BCMA双抗获批上市。目前共有2款CD3/BCMA双抗上市产品,分别为强生/Genmab的Teclistamab以及辉瑞的Elranatamab,均被FDA批准用于治疗复发或难治性(R/R)多发性骨髓瘤(MM)患者。
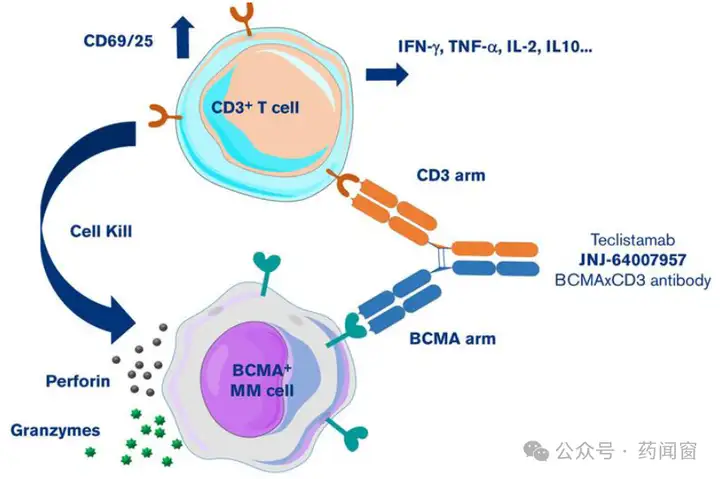
图9 CD3/BCMA作用机制(Teclistamab为例)
Teclistamab疗效略优,Elranatamab安全性更佳。在已上市的两款CD3/BCMA双抗中,Teclistamab在疗效方面略占优势(肩并肩比较),其ORR为61.8%,CR为28.2%,而Elranatamab的ORR为57.7%,CR为25.8%。在安全性方面,Teclistamab 的细胞因子释放综合征(CRS)发生率为72%,而Elranatamab的CRS发生率仅为58%,总体而言Elranatamab安全性优于Teclistamab(肩并肩比较)。
表6 CD3/BCMA双抗上市产品获批数据对比

表7 CD3/BCMA双抗研究进展

CD3/GPRC5D双抗
GPRC5D是一种孤儿G蛋白偶联受体,其在MM细胞表面高表达,而正常组织表达有限(通常仅限于毛囊),研究表明65%的多发性骨髓瘤患者GPRC5D有超过50%的表达阈值。GPRC5D激活多个信号通路,包括细胞增殖、生存和迁移的途径,促进MM细胞的生长和扩散。
独立于BCMA表达。GPRC5D在MM细胞中独立于BCMA特异性高表达,既可单靶向也可双靶向开发治疗药物,使得GPRC5D成为继BCMA后又一极具潜力的MM治疗靶点。
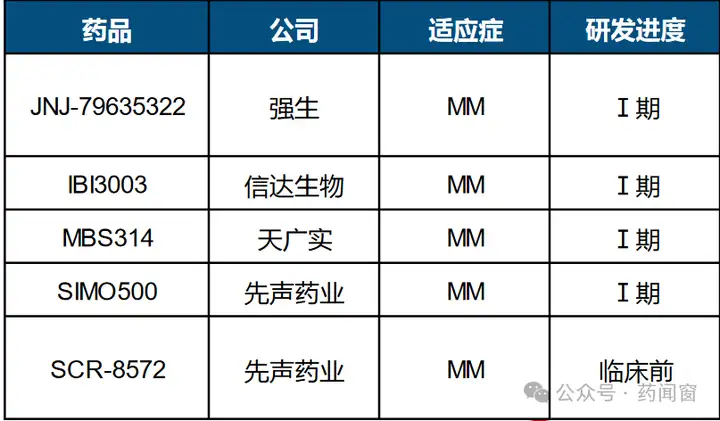
1款靶向GPRC5D双抗上市。目前全球已有1款CD3/GRPC5D双抗获批上市,即强生/Genmab的Talquetamab,被FDA批准用于治疗既往接受过至少四线治疗的复发或难治性多发性骨髓瘤患者。
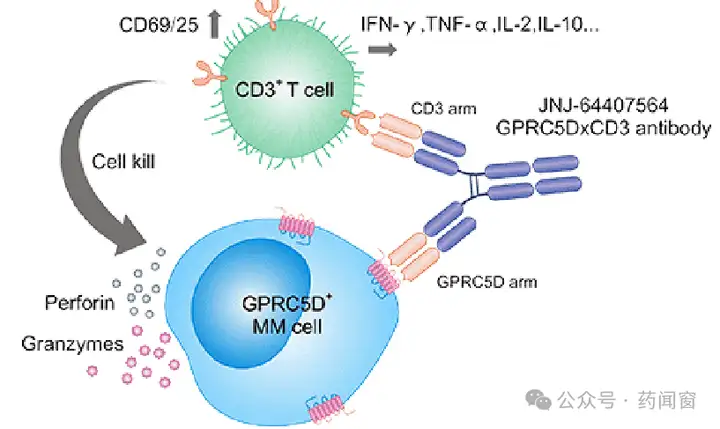
图10 CD3/BCMA作用机制(Teclistamab为例)
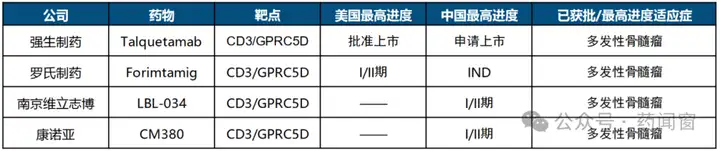
表8 CD3/GPRC5D双抗研究进展
CD3/BCMA/GPRC5D三抗
BCMA与GPRC5D靶标的表达异质性。MM细胞针对BCMA和GPRC5D的表达展现出明显的异质性特征,且单阳性肿瘤细胞占比较高。基于这一特性,BCMA/GPRC5D/CD3三抗理论上可同时靶向BCMA单阳性及GPRC5D单阳性MM细胞,从而实现有效杀伤,预期能实现较双抗更高的缓解率。据强生开展的Teclistamab与Talquetamab联合治疗的临床试验结果显示,联用方案ORR达到84%(CR 34%),且未显著增加安全性风险。
三抗具备潜在抗耐药优势。在双抗长期治疗MM的临床实践中,部分患者会出现耐药现象,其主要机制之一为靶抗原(如BCMA或GPRC5D)的丢失或下调。鉴于此,双靶向的三抗理论上能够更有效地克服双抗面临的耐药挑战,延缓耐药现象的出现时间。
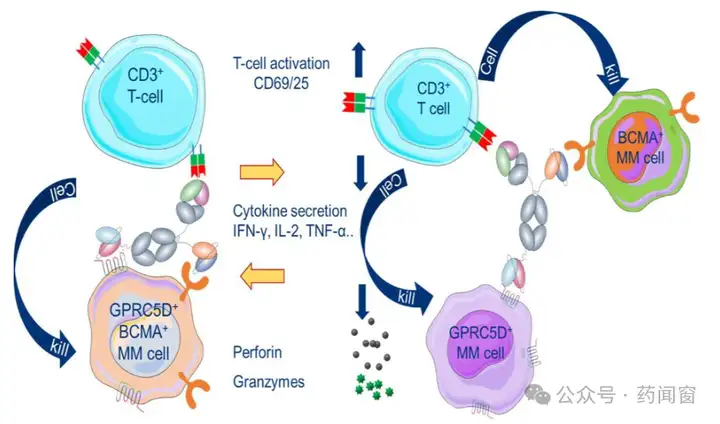
图11 CD3/BCMA/GPRC5D三抗作用机制
表9 CD3/BCMA/GPRC5D三抗研究进展
CD3/DLL3双抗
Amgen的Tarlatamab(CD3/DLL3)在后线SCLC患者中展现优异疗效。Tarlatamab设计为Single chain,整体更亲和DLL3。Tarlatamab是一种偶联了IgG Fc片段的双特异性T细胞接合剂(BiTE)抗体,外侧scFv靶向小细胞肺癌(SCLC)肿瘤中选择性表达的delta样配体3(DLL3),内侧scFv靶点T细胞表面表达的CD3蛋白。在专利中,Tarlatamab对DLL3的亲和力为6.4×10-10M,对CD3的亲和力为1.49×10-8M
Tarlatamab在三线ES-SCLC患者中展现优异突出疗效,产品已于24年5月经美国FDA批。
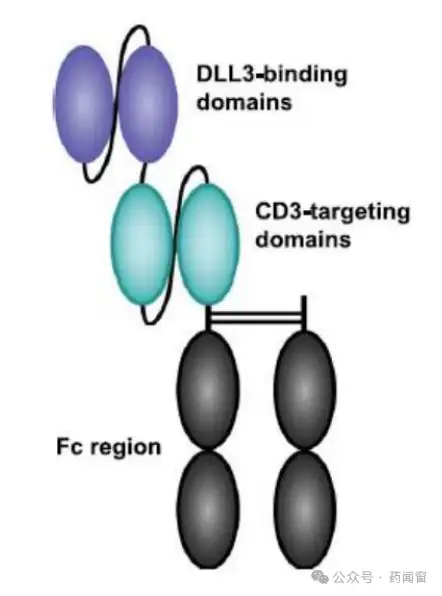
图12 Tarlatamab结构
Tarlatamab用药后,响应患者的持续有效时间长,mDoR达到9.7个月,从而显著提升患者总生存期。其中响应最久的患者接近70个月还未进展,响应时间在40个月以上的患者有17人,占据响应患者的约50%。整体看,Tarlatamab用药后的长DOR时间让部分患者获益明显,从而提升生存时间。
CD3/PSMA双抗
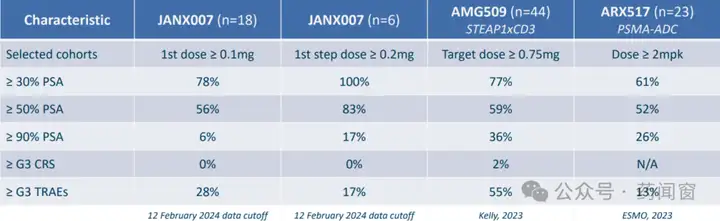
2024年2月26日,Janux Therapeutics公布PSMA/CD3双抗JANX007治疗前列腺癌数据。公司技术特点为前抗体技术,技术平台为TRACTr。药代动力学研究表明TRACTr注射后肿瘤特异性的有效活化。产品取得初步PSA响应,后续rPFS结果值得关注。
表10 CD3/PSMA类双抗药物疗效对比
CD3/CLDN18.2双抗
CLDN18.2(Claudin18.2)是一种在胃、胰腺和其他实体瘤中广泛表达的肿瘤相关抗原,其在所有胃癌、胰腺癌患者中的阳性率可以达到近60%,是近年来实体瘤领域研究最火热的靶点之一。
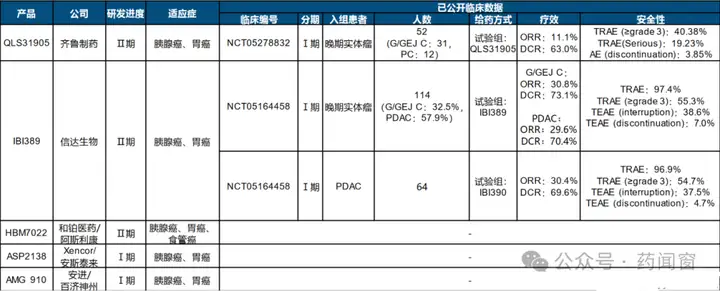
共5款CD3/CLDN18.2双抗进入临床研究阶段。目前,齐鲁制药QLS31905和信达生物IBI389已公布Ⅰ期临床结果,显现出初步的疗效和可控的安全性。
表11 CD3/CLDN18.2双抗临床研发进展
CD3/EGFR双抗
EGFR(表皮生长因子受体)是一种跨膜酪氨酸激酶受体,位于细胞膜上,属于酪氨酸激酶受体家族。EGFR在多种癌症中过表达或发生突变,包括非小细胞肺癌(NSCLC)、胶质母细胞瘤、结直肠癌(CRC)、乳腺癌、卵巢肿瘤等。特别在NSCLC中,EGFR的突变率很高(全球平均约35%,中国达到40%)。
共26款CD3/EGFR多抗进入临床研究阶段,共计12项药物实体瘤临床试验获批,全球临床稳步推进中。
表12 CD3/EGFR双抗临床进展

CD3/HER2双抗
HER2即人表皮生长因子受体2,与EGFR同属酪氨酸激酶受体家族,在多个癌种中高度表达。HER2高表达在乳腺癌中检出率15%~25%,肺癌中的检出率约2.5%,胃癌检出率约20%,胆管癌检出率约20%,卵巢癌检出率约27%,子宫内膜癌中检出率约18%~80%。
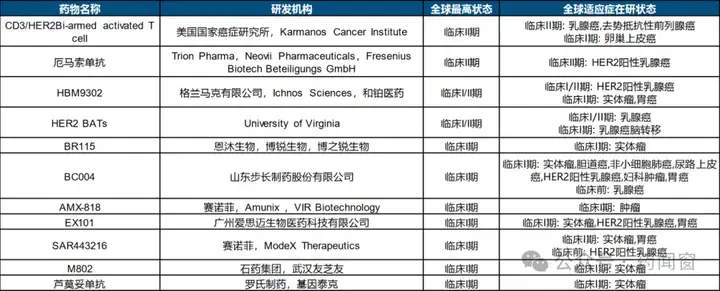
共29款CD3/HER2双抗进入临床研究阶段。其中,11款产品步入临床I/II期阶段。
表13 CD3/HER2双抗临床进展
随着对CD3机制的理解成熟以及TAA的逐步探索,TCE类药物有望展现更多潜在可能。作为肿瘤免疫类药物的新机制,TCE类药物已逐步在血液瘤中站稳脚跟,并在向实体瘤和自免适应症突破。
【关于逐典】
上海逐典生物科技有限公司,坐落于中国(上海)自由贸易试验区,获得ISO9001质量体系认证,是一家从事重组蛋白研发和销售的高新科技企业。
逐典生物始终秉持以客户为中心的理念,针对重组蛋白的结构设计、纯化工艺及其稳定剂型相关的多项关键技术进行优化。专业定向蛋白变复性技术,可将大肠杆菌大量表达的变性固体蛋白转变成高活性可溶性蛋白。凭借技术优势,逐典生物新品研发周期短且可控性强,为重组蛋白的高质高效研发提供保障,为企业生产降本增效。
公司自成立以来成功开发百余种高活性细胞因子及多种高活性蛋白酶,覆盖细胞培养、病毒纯化以及质量分析等生物工艺各个环节。可广泛应用于科研、医药生产及IVD(体外诊断试剂)等领域,满足各类用户所需。
