产品中心
技术交流

扫描二维码
Cell重磅一个细胞免疫全过程之——“巨噬细胞”
来源:生信人
巨噬细胞(Macrophages)是固有免疫系统的重要组成部分,可以根据免疫微环境中不同刺激信号呈现不同的功能状态,具有极高的可塑性,这一过程现象被称为巨噬细胞极化(macrophage polarization)。
巨噬细胞极化类型和功能:
M1型(经典激活):具有促炎、抗菌、抗肿瘤功能,分泌IL-6、IL-12、ROS等促进Th1免疫应答。
M2型(替代活化):M2a:参与寄生虫免疫、组织修复;M2b:免疫复合物/TLR激动剂诱导,免疫调节;M2c:IL-10/糖皮质激素诱导,免疫抑制;M2d:肿瘤相关,促血管生成。
信号通路:
M1通路:TLR/NF-κB通路;STAT1通路
M2通路:STAT6/PPARγ通路;IRF4/AMPK通路(调控代谢重编程和M2相关基因)
代谢特征:
M1:依赖糖酵解(Warburg效应),产生ATP和乳酸。
M2:依赖氧化磷酸化和脂肪酸氧化,线粒体活性增强。
当以巨噬细胞极化“macrophage polarization”在CNS(Cell、Nature、Science)杂志上检索近一个月接受发表文章,发现Cell及子刊共计87篇,Nature 及子刊共计121篇;Science及子刊共计13篇。

跟着CNS的脚步,让我们一起来探索巨噬细胞极化与免疫微环境的关系吧~
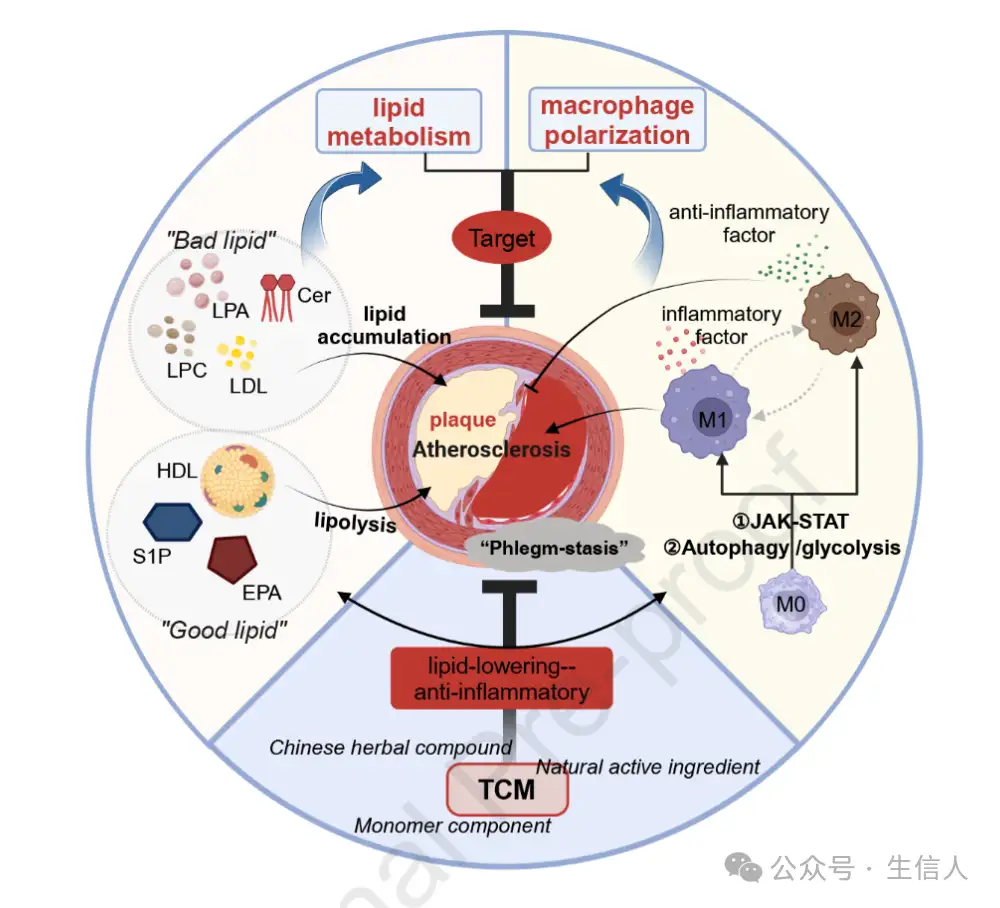
一、动脉粥样硬化中脂质代谢与巨噬细胞极化的相互作用

本文深入探讨了动脉粥样硬化(AS)进程中脂质代谢与巨噬细胞极化之间的相互作用关系。AS是一种慢性炎症性疾病,脂质代谢异常和巨噬细胞功能失调在其发生发展中至关重要。巨噬细胞作为脂质代谢和炎症反应的关键参与者,其极化状态与脂质代谢密切相关,二者相互影响,共同推动AS进展。
氧化型低密度脂蛋白(ox - LDL):ox - LDL是AS发生发展的关键因素,它可通过 Toll 样受体(TLR)、清道夫受体等途径激活巨噬细胞,促使其向促炎的M1型极化,分泌白细胞介素-6(IL - 6)、肿瘤坏死因子-α(TNF - α)等促炎细胞因子,加剧炎症反应,促进AS发展。
脂肪酸(FAs):不同类型FAs对巨噬细胞极化影响各异。饱和脂肪酸可激活核因子-κB(NF-κB)信号通路,诱导巨噬细胞向M1型极化;而不饱和脂肪酸,如ω-3多不饱和脂肪酸,能通过激活过氧化物酶体增殖物激活受体(PPAR)等途径,促进巨噬细胞向抗炎的M2型极化,发挥抗AS作用。
巨噬细胞极化调控脂质代谢
M1型巨噬细胞:M1型巨噬细胞高表达清道夫受体,如CD36,大量摄取ox-LDL,形成泡沫细胞,促进脂质在血管壁内沉积。同时,M1型巨噬细胞分泌的炎症因子会干扰胆固醇逆向转运相关蛋白的表达和功能,阻碍胆固醇从血管壁清除,加重脂质代谢紊乱。
M2型巨噬细胞:M2型巨噬细胞表达较多的载脂蛋白E(ApoE)和胆固醇转运蛋白ABCA1,促进胆固醇逆向转运,将血管壁内的胆固醇转运至肝脏进行代谢清除,改善脂质代谢,抑制AS进展。
相互作用的分子机制:PPAR家族、肝X受体(LXR)等核受体在脂质代谢与巨噬细胞极化的相互调控中起关键作用。PPAR激活后,一方面调节脂质代谢相关基因表达,另一方面抑制 NF-κB信号通路,减少促炎细胞因子分泌,促使巨噬细胞向M2型极化LXR可通过调控ABCA1等胆固醇转运蛋白表达,影响脂质代谢,同时调节巨噬细胞极化相关基因,抑制炎症反应。
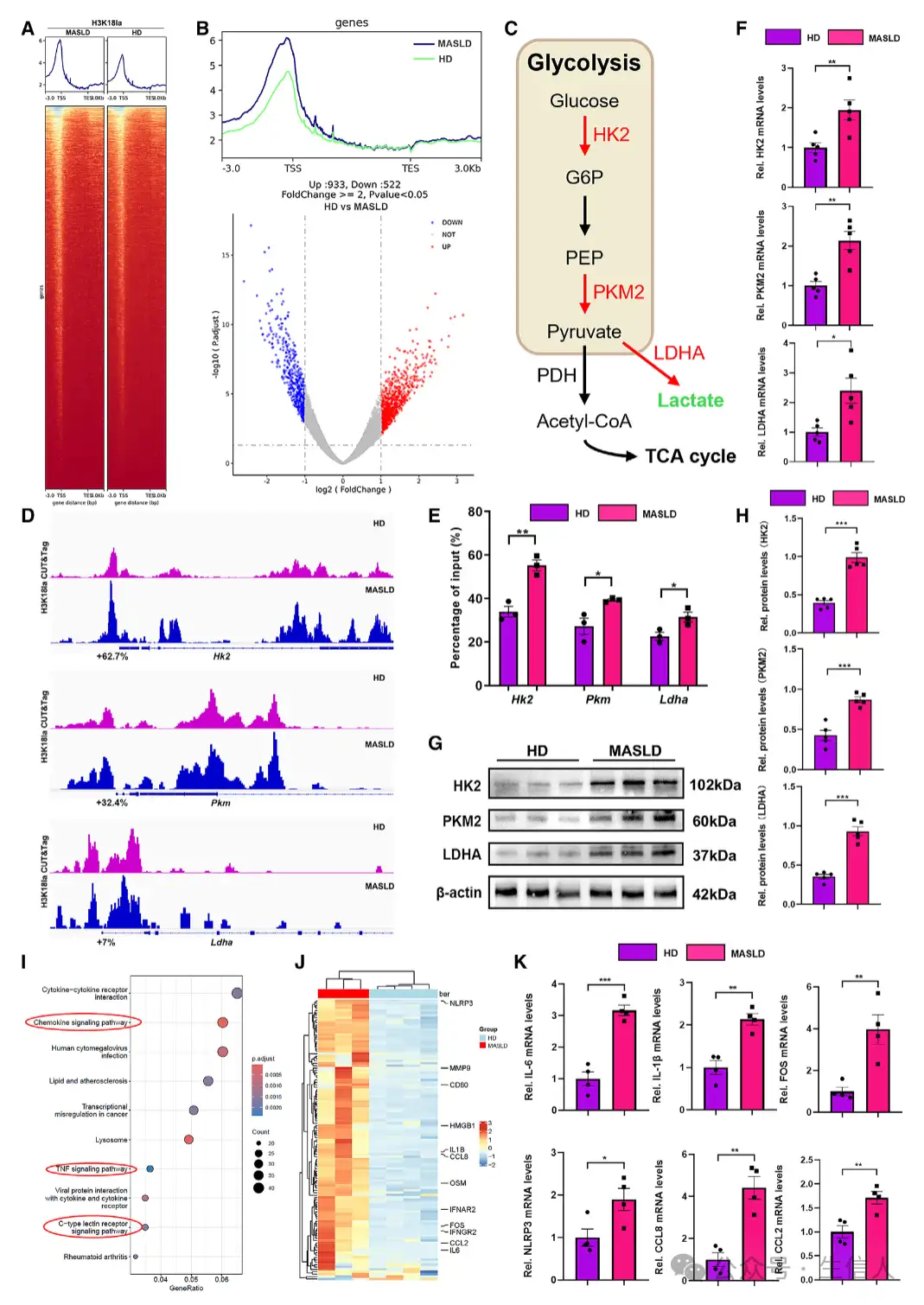
二、MASLD中己糖激酶2通过组蛋白乳酸化介导的肝脏巨噬细胞代谢应激和炎症负担

本文揭示了己糖激酶2(HK2)通过组蛋白乳酸化介导肝脏巨噬细胞代谢应激和炎症反应。研究铜鼓细胞和动物模型实验,验证了HK2的作用。

三、瓜氨酸调节小鼠巨噬细胞代谢和炎症以对抗衰老

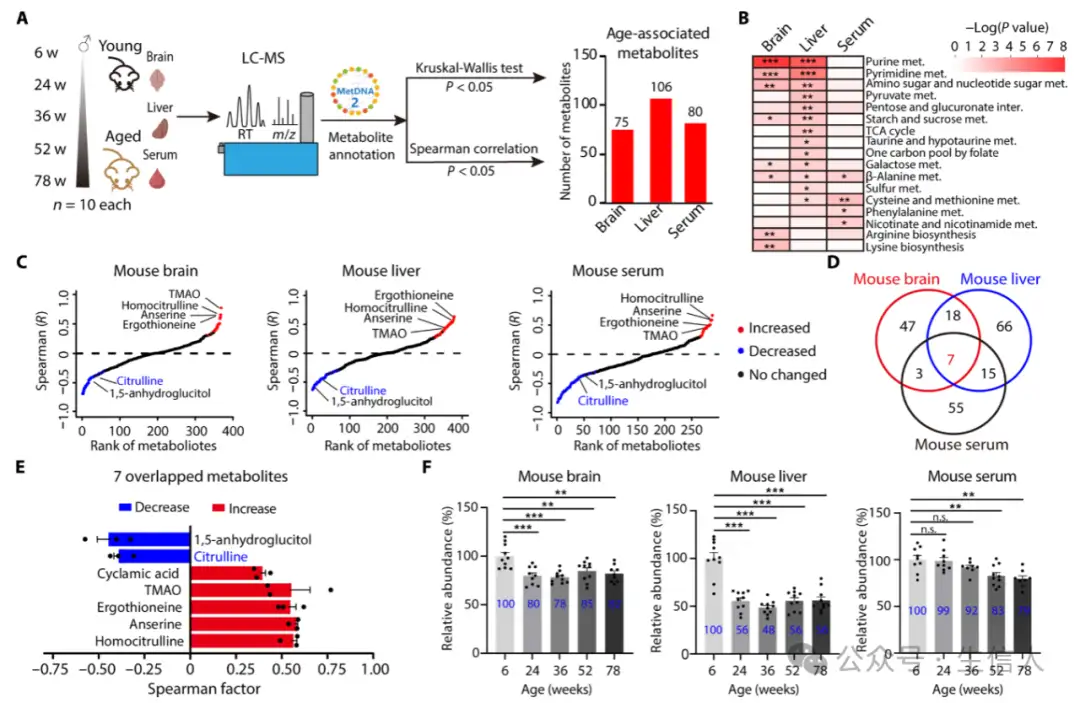
研究人员对不同年龄小鼠的脑、肝组织和血清进行非靶向代谢组学分析,发现瓜氨酸随衰老显著下调(图1)。为探究其作用,在体外实验中,用活性氧诱导细胞衰老模型处理小鼠胚胎成纤维细胞,补充瓜氨酸可减少DNA损伤、抑制衰老相关β-半乳糖苷酶活性、降低衰老相关炎性细胞因子水平。在原代骨髓来源的巨噬细胞(BMDMs)实验中也得到类似结果,且这些效果在年轻细胞中不明显。
体内实验中,给老年小鼠长期补充瓜氨酸,能降低体重、减轻脾脏和肝脏重量,减少炎症,改善衰老相关表型(图3)。进一步研究发现,瓜氨酸是炎症的内源性代谢拮抗剂,能调节巨噬细胞代谢和炎症。巨噬细胞在衰老过程中,其抗炎功能失调,而瓜氨酸可通过调节 mTOR-HIF1α-糖酵解信号通路,抑制巨噬细胞的促炎反应,对巨噬细胞极化产生影响(图5)。
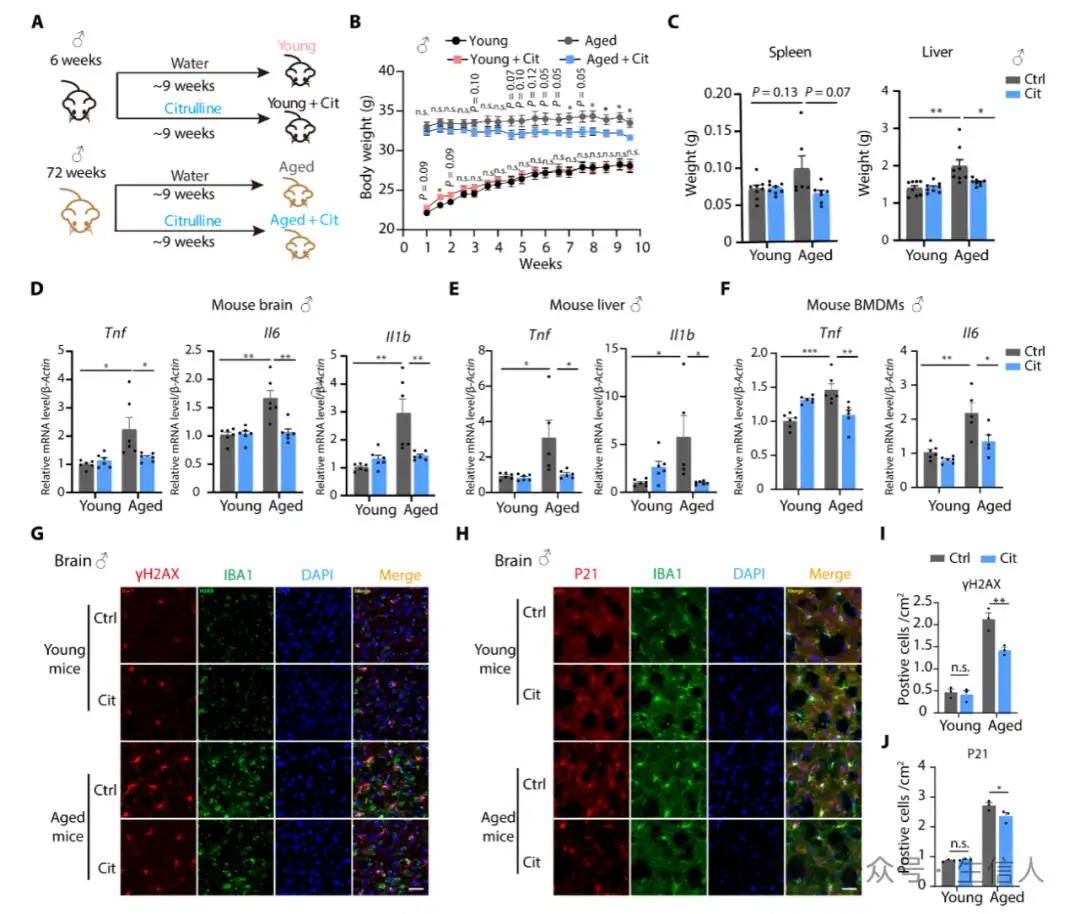
图3
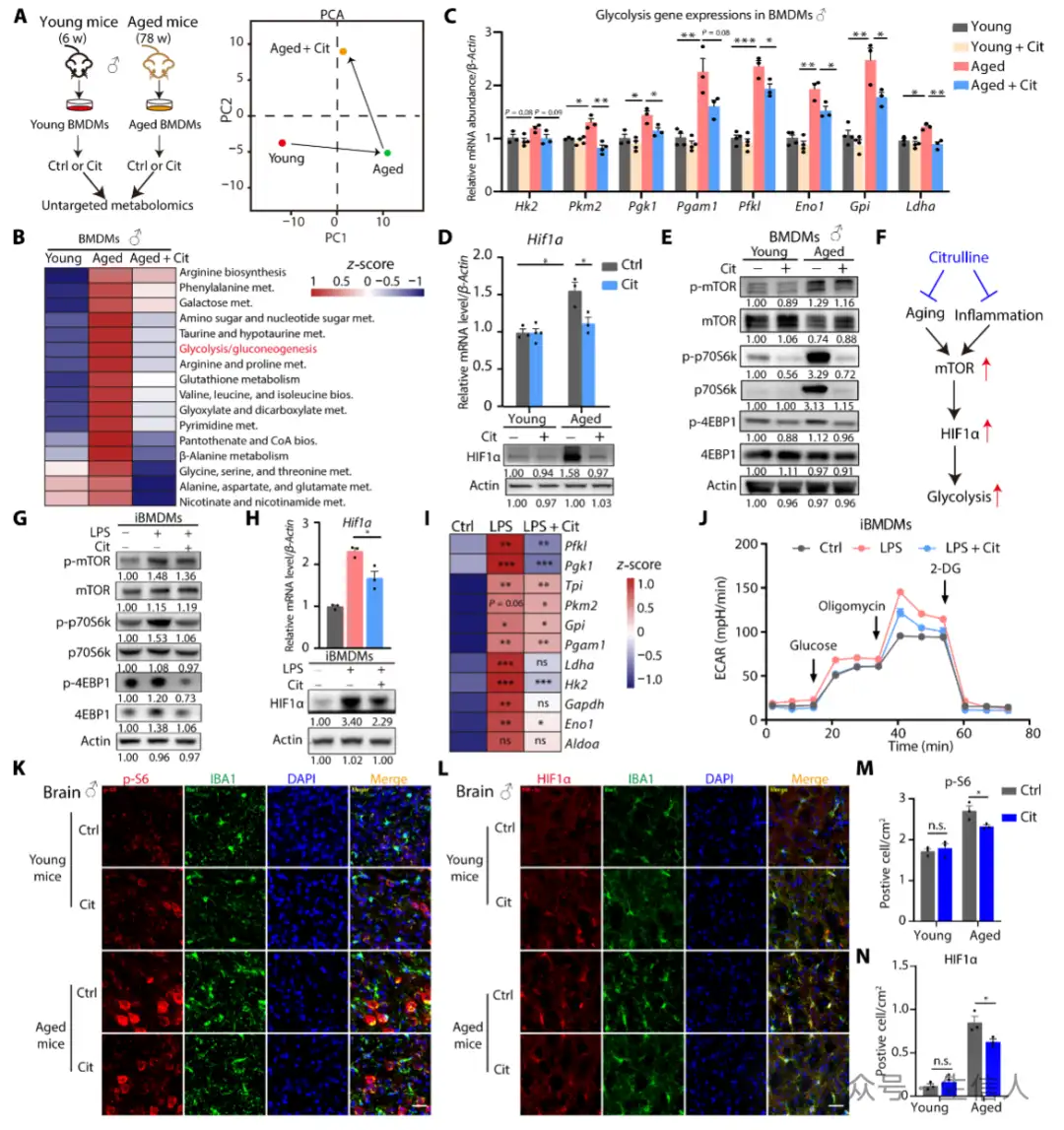
图5
研究还揭示衰老时巨噬细胞中瓜氨酸缺乏是由于Nos2表达下降。这项研究表明,瓜氨酸补充剂有望成为对抗衰老相关变化的有效疗法。不过,研究仅以雄性小鼠为模型,未来还需研究性别因素对代谢变化的影响