产品中心
技术交流

扫描二维码
一文读懂:生物类似药在癌症治疗中的应用与前景
来源:生物制品圈
生物类似药是与生物药(即原研生物制剂)在结构和功能上相似的药物 。生物药源自活细胞和微生物,如动物细胞、组织、酵母和细菌等 。与普通仿制药不同,生物类似药并非简单的复制品,但其成本比原研生物药低,在促进制药行业竞争、让患者能用上必需药物方面发挥着关键作用 。它的出现,为医疗领域带来了新的选择,有望改善患者的治疗体验和医疗资源的分配 。
生物类似药在治疗多种慢性疾病方面,与生物药一样有效、安全和纯净,可用于治疗肾衰竭、生长障碍、炎症性消化疾病、糖尿病、癌症、关节炎、肠道疾病等 。生物药的发展可追溯到 20 世纪,21 世纪其重要性日益凸显 。自 2006 年欧洲批准首个生物类似药 omnitrope(生长激素)以来,欧美批准的生物类似药数量不断增加 。生物药和生物类似药在多个方面存在差异,生物药结构更为复杂,其氨基酸序列和三维结构复杂,且在合成后还会通过糖基化等过程进行修饰 。相比之下,生物类似药在生产过程中虽力求与原研药相似,但因生产工艺等因素,两者仍存在一定区别 (原文 Table 1,对比生物类似药和生物药在多个方面的差异,包括研发成本、安全性、适用疾病、生产复杂性和举例等,让读者更直观地了解两者区别)。不同监管机构对生物类似药的审批和监管制定了详细指南 。美国食品药品监督管理局(FDA)从分析、临床、免疫原性和药理学等多方面评估生物类似药;欧洲药品管理局(EMA)则对比较定性、临床前和临床研究提出要求,并考虑适应症外推;世界卫生组织(WHO)和加拿大卫生部也分别为生物类似药的规范发展提供指导 。这些指南旨在确保生物类似药的质量、安全性和有效性,同时促进生物类似药市场的健康发展 。此外,生物类似药的互换性也是监管关注的重点,不同国家对其规定有所不同,有些国家允许或鼓励生物类似药的替换以节省成本,而有些国家则需要处方医生明确批准 。目前,美国已批准多种生物类似药用于癌症治疗,如 filgrastim、bevacizumab - awwb、trastuzumab dkst、pegfilgrastim - jmdb 等,这些药物在治疗不同类型癌症方面发挥着重要作用 。

许多国家药品机构(NMAs)网站对生物类似药的信息提供情况参差不齐,部分国家在这方面的信息更全面 。尽管欧盟在评估和批准生物类似药方面成绩显著,使得大量生物类似药在欧盟范围内获批上市,但欧洲医疗保健提供者和患者(EHPPs)对生物类似药仍存在认知不足和信任问题,这表明人们对生物药和生物技术的理解还需加深 。获取生物类似药的开发信息对医疗专业人员和患者都至关重要 。目前癌症治疗面临着成本高、药物可及性差等问题,生物药虽在肿瘤治疗中效果显著,但价格昂贵,许多患者难以承受 。生物类似药的出现带来了价格竞争,有助于降低治疗成本 。据估计,2016 - 2022 年,仅欧盟 5 国使用生物类似药就能节省超过 100 亿欧元,美国若推出 11 种生物类似药,未来 5 年医疗保健成本有望降低 2500 亿美元 。
不同生物类似药的成本效益有所差异,其成本与生物药的成本比值在 59.4% - 86.0% 之间 。使用生物类似药 1 个月的成本估计在 322 美元至 7424 美元之间,而每位患者的总治疗成本约为 17578 美元至 38923 美元 。在英国,Filgrastim - Biosimilar 的推出使药物使用率增加了 104%;在欧洲,2007 - 2014 年 Epoetin - Biosimilars 的出现,使罗马尼亚和保加利亚的治疗量增长了 263%,价格下降了 50% 。这些数据充分显示了生物类似药在降低医疗成本、提高药物可及性方面的重要作用 。
在美国,目前有 6 种生物类似药被批准用于治疗 TNF - 1,但仅有 2 种广泛可用 。一项针对溃疡性结肠炎或克罗恩病患者的研究评估了生物类似药的使用情况和患者对其的态度 。研究发现,虽然超过 80% 的胃肠病学家愿意开具生物类似药处方,但患者对将其作为一线治疗存在犹豫,79% 的患者对治疗效果表示满意,69% 的患者对症状控制表示满意,不过仍有 35% 的患者对使用生物类似药或生物药治疗没有顾虑 。胃肠病学家表示,生物类似药在生物疗法中占比 12% - 13%,在所有药物中占比 4% - 5% ,且大多数(88%)更倾向于使用原研生物药 。当被问及开具生物类似药的原因时,89% 的医生表示想体验新产品,44% 的医生认为其具有疗效、成本效益和经济稳定性等优势 。这一研究结果表明,生物类似药在胃肠道疾病治疗中的接受度有待提高,需要加强对患者的教育,增进医患之间的沟通,让患者更好地了解生物类似药的重要性和优势 。
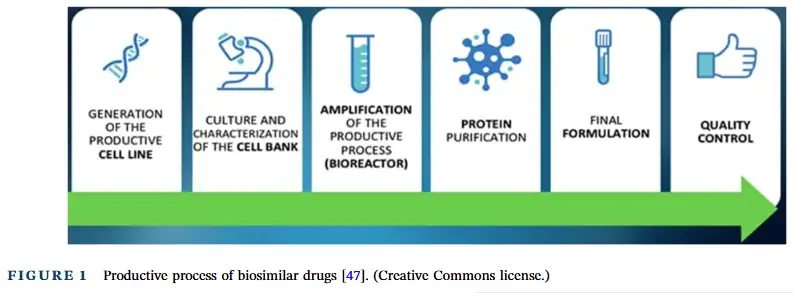
生物类似药的开发采用了先进的治疗方法,与化学驱动的药物不同,它主要涉及复杂的肽、蛋白质和糖蛋白,以全新的方式治疗疾病 。其开发过程需要进行临床前表征和药代动力学 / 药效学评估,以确保与原研药的相似性和安全性 。生物类似药的生产是一个系统的过程,主要包括三个关键步骤(原文 Figure 1,展示生物类似药的生产流程,从细胞系的建立、培养扩增,到蛋白质的纯化、制剂和质量控制,让读者清晰了解生产过程)。第一步是确定参考产品的属性,包括细胞的扩增和生物产品的表达,以及评估生物产品的相似性、分离和纯化蛋白质并确定制剂;第二步是明确生物类似药的目标质量属性、临床有效性和效力,同时检测其与参考产品的差异,以保证药代动力学相似性;第三步是对生物类似药进行严格的开发过程和逐步的可比性测试,确保与参考产品相比,任何差异都不会影响产品的临床性能 。生物类似药和仿制药虽都能提供低成本的选择,但两者存在显著差异 。生物类似药大多由活细胞系统生产,如利用大肠杆菌等细菌,通过重组 DNA 技术合成蛋白质 。在生产过程中,即使是温度、营养物质和 pH 值等微小差异,也可能影响药物的结构、功能和安全性 。而仿制药的活性成分通常较小,更容易复制和生产 。例如,许多由大肠杆菌生产的药物,如 filgrastim、IFN α2a、IFN α2b 等,被用于治疗癌症、艾滋病相关的中性粒细胞减少症、白血病等疾病 。
单克隆抗体在免疫疗法中具有重要作用,因其能够激活免疫系统对抗癌症 。它可以识别并靶向消灭外来病原体和癌细胞,例如,rituximab 能与 B 细胞上的蛋白质 CD20 结合,从而杀死癌细胞;blinatumomab 则通过结合 B 细胞上的 CD19 和 T 细胞上的 CD3,帮助 T 细胞靶向杀死白血病细胞 。下面介绍几种常见的单克隆抗体生物类似药在癌症治疗中的具体作用 。
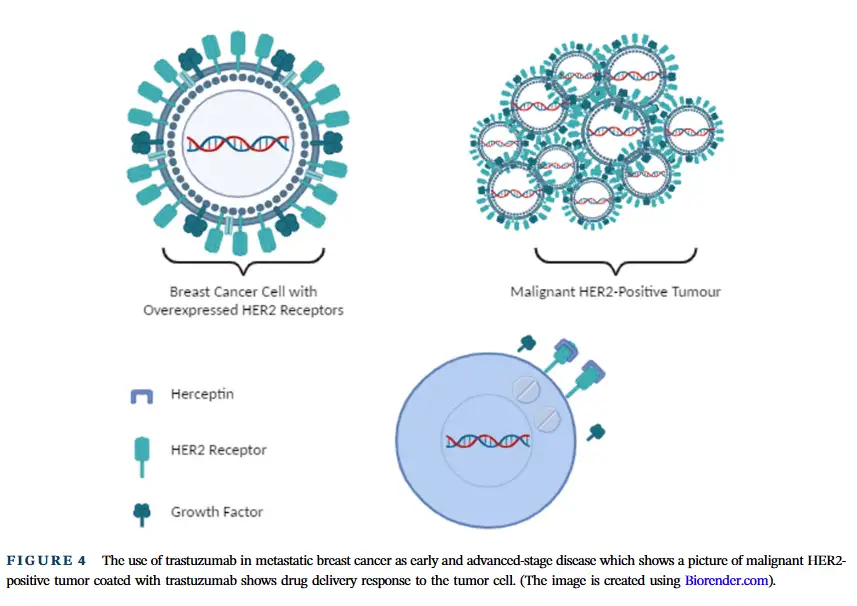
Herceptin(曲妥珠单抗)及其生物类似药 ogivri:Herceptin(曲妥珠单抗)主要用于治疗 HER2 阳性乳腺癌 。在正常细胞中,HER2 等受体参与细胞生长和增殖的信号传导 。但在 HER2 阳性乳腺癌细胞中,HER2 受体数量过多,会导致细胞生长信号过度激活,从而引发癌症 。曲妥珠单抗能够特异性地结合 HER2 受体,阻止其形成二聚体,进而抑制细胞内的信号传导,阻碍癌细胞的生长 (原文 Figure 4,展示曲妥珠单抗在转移性乳腺癌中的作用机制,即与 HER2 受体结合,阻止癌细胞生长,帮助读者理解其作用原理)。此外,抗体 - 药物偶联物 “Trastuzumab deruxtecan” 已获批用于治疗先前接受过至少两种针对 HER2 治疗方案的癌症患者 。一项临床试验表明,与 “Trastuzumab emtansine” 相比,“Trastuzumab deruxtecan” 在治疗转移性乳腺癌方面更具优势 。
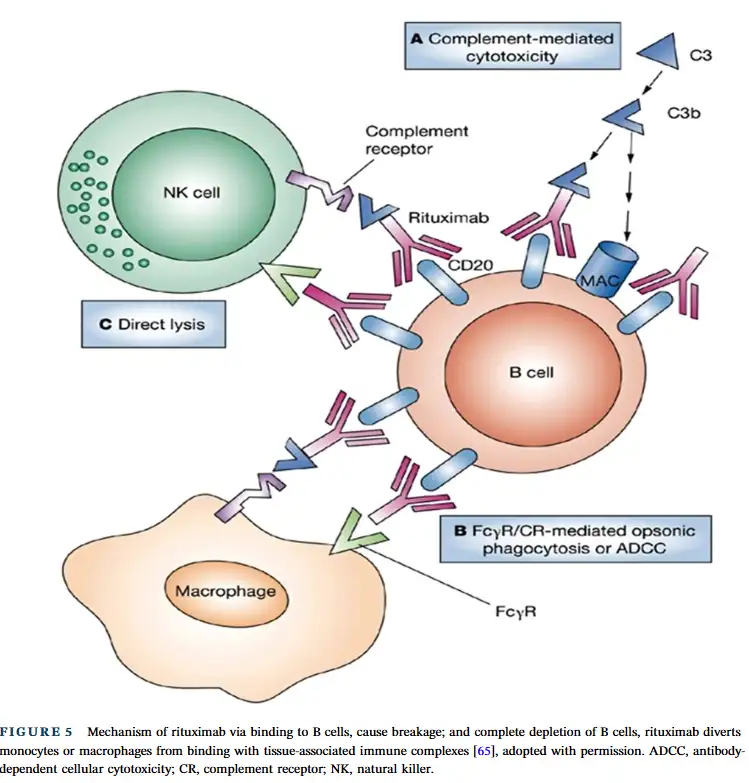
Rituximab(利妥昔单抗):Rituximab(利妥昔单抗)是一种靶向 B 细胞表面 CD20 蛋白的抗体,主要用于治疗非霍奇金淋巴瘤、类风湿关节炎和自身免疫性溶血性贫血等疾病 。它通过与 CD20 蛋白结合,能够抑制 B 细胞的功能,从而达到治疗疾病的目的 。在使用 Rituximab 治疗前和治疗过程中,需要进行多项检测,如肝炎检测和结核病检测等,以确保治疗的安全性 。首次给药通常需要在医院或门诊输液室进行静脉输注,且治疗过程中需使用类固醇、对乙酰氨基酚和抗组胺药等,以减少过敏反应的发生 (原文 Figure 5,展示利妥昔单抗与 B 细胞结合,引发补体介导的细胞毒性作用、抗体依赖的细胞介导的细胞毒性作用等,从而清除 B 细胞的机制)。不过,Rituximab 也存在一些副作用,如可能导致身体对某些疾病的易感性增加,还可能引发血小板聚集减少、进行性多灶性白质脑病等严重不良反应 。
Adalimumab 和 Infliximab(抗 TNF 治疗药物):Adalimumab 和 Infliximab 都是针对细胞因子 TNF - α 的单克隆抗体 。TNF - α 在炎症反应中起着关键作用,与多种炎症性疾病的发生发展密切相关 。这两种药物通过靶向 TNF - α ,能够减轻炎症反应,在治疗炎症性肠病、类风湿关节炎和银屑病等疾病方面具有显著疗效 。其中,Infliximab 的临床开发最初在小鼠身上进行,之后经过改造使其更适用于人体 。常见的品牌名有 Remicade、Remsima、Renflexis 和 Avsola 等 。使用 Remicade 治疗时,通常在治疗开始时(0 - 6 周)进行静脉输注,之后在治疗结束时(8 周)每 8 周进行一次维持治疗,每次输注持续 2 小时 。
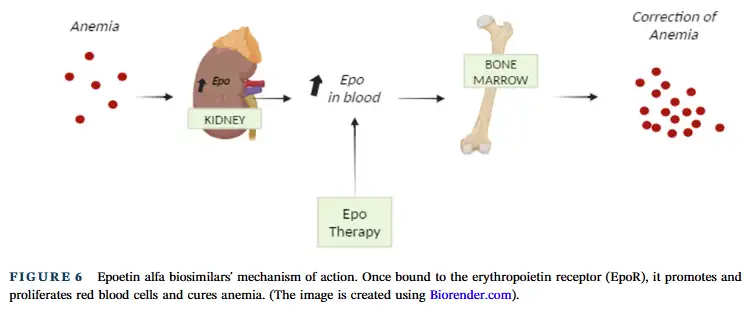
化疗诱导的贫血是癌症治疗中常见的并发症,会严重影响患者的生活质量 。Epoetin alfa 生物类似药通过临床前表征和药效学研究开发而来,在适当的药物监测下,对治疗贫血具有显著效果 。慢性肾病患者中贫血的发生率较高,且对健康相关生活质量的影响较大 。在开发 Epoetin alfa 生物类似药时,需要进行一系列的分析和评估,以确保其与原研药的相似性和安全性 。临床研究表明,生物类似药 Epoetin 与原研药在药效学方面具有相似性,为贫血患者提供了更多的治疗选择 。Epoetin(促红细胞生成素)与其受体(EpoR)的相互作用对于促进红细胞的生成和存活至关重要 。通过使用红细胞白血病细胞系等研究手段,可以深入了解生物类似药对红细胞祖细胞的作用机制 (原文 Figure 6,展示 Epoetin alfa 生物类似药的作用机制,即与促红细胞生成素受体结合,促进红细胞的生成和增殖,纠正贫血)。
生物类似药在肿瘤学实践中发挥着越来越重要的作用,例如 filgrastim 和 epoetin 等生物类似药,不仅具有抗癌作用,还能提高患者的健康水平 。对于肿瘤学家来说,从原研生物产品转换使用生物类似药,主要担忧的是疗效降低和出现不良事件,以及生物药的临床改变可能诱导免疫原性 。然而,大量研究证明,生物类似药不仅在癌症治疗中安全有效,在治疗克罗恩病、结肠炎等其他疾病方面也有良好表现 。
生物类似药相较于参考产品具有成本优势,多种免疫疗法与生物类似药联合使用,展现出了良好的预防效果 。如 filgrastim 用于预防化疗引起的(发热性)中性粒细胞减少症,obinutuzumab 用于治疗滤泡性淋巴瘤,pembrolizumab 用于治疗肺癌等 。肿瘤治疗中的生物类似药在随机试验中,展现出与参考药物相似的肿瘤反应和疗效 。例如,曲妥珠单抗生物类似药用于治疗乳腺癌或转移性胃腺癌,经过三期试验后获批,在 24 周的治疗中表现出良好的效果 。
在癌症诊断方面,高通量计算分析和 “片段组学” 等新的 “组学” 研究,为血液检测和肝癌检测带来了新方法 。通过检测 DNA 片段,利用机器学习技术可以区分癌症亚型,发现与肿瘤相关的基因表达变化 。循环肿瘤 DNA(ctDNA)和细胞游离 DNA(cfDNA)分析在癌症诊断和监测中具有重要意义,能够检测肿瘤的突变、监测癌症复发,还可以通过检测 AKT 和 PIK3CA 等基因的突变,为癌症治疗提供指导(原文 Figure 8,展示 cfDNA 分析在检测转移性病变中的应用,包括突变特征分析、染色体易位分析等多种检测方法及应用方向)。
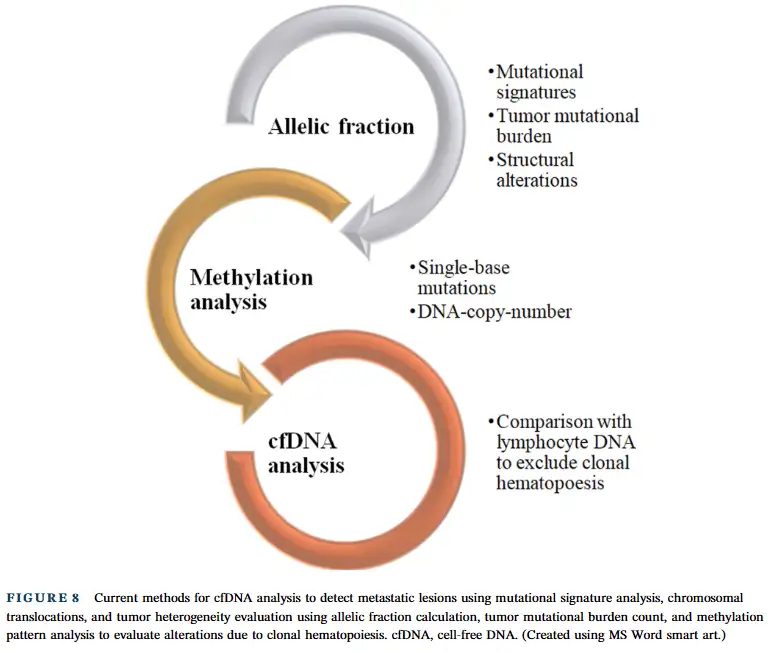
液体活检技术将片段组学与突变和表观遗传变化相结合,可用于多种癌症的早期检测,如肺癌、结肠癌和乳腺癌等,通过多癌症筛查能够早期发现异常有丝分裂的后果 。cfDNA 分析作为一种快速发展的早期诊断方法,能够在周边血液中检测到肿瘤特异性的变异,作为一种生物标志物,为癌症的早期诊断和治疗提供了重要依据 。
新一代测序(NGS)技术通过大规模测序和高通量计算分析,结合多种组学研究,推动了肿瘤学从基于肿瘤部位的分类向基于癌症分子的分类转变 。该技术涵盖核酸分离、DNA/RNA 片段化、文库制备与测序、扩增以及数据注释等多个步骤,能够对多个基因进行高通量测序,检测出罕见的变异,从而更容易发现患者的基因突变,为个性化医疗和癌症治疗提供了有力支持 (原文 Figure 9,展示通过 NGS 的多组学网络分析,包括基因组、转录组、蛋白质组等,对肿瘤进行分子特征分析,以实现精准医疗)。
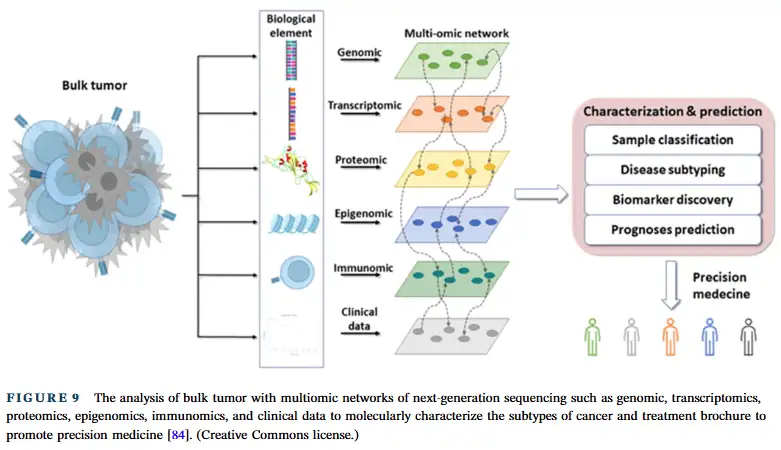
在癌症研究中,NGS 技术可用于多种癌症的基因检测,如确定卵巢癌中的体细胞突变、评估宫颈癌、甲状腺癌、外阴癌和唾液癌的肿瘤突变负荷等 。此外,它还能揭示肿瘤与宿主免疫系统之间的相互作用,为癌症的进展、分子机制研究以及肿瘤免疫微环境的生物标志物发现提供重要信息 。通过对多组学数据的分析,可以预测疾病亚型和疾病进展,为精准医疗提供依据,有望将癌症治疗的成功率提高 10 倍 。
生物产品的复杂性使得生物类似药比化学药物更为复杂,这对制造商和处方医生提出了更高的要求 。在生物类似药上市后,需要进行严格的监测,评估其疗效和安全性 。目前,市场上的 33 种生物类似药中,有 17 种用于癌症治疗,3 种用于自身免疫性疾病,1 种用于糖尿病 。未来,随着监管机构对生物类似药安全性和有效性的信心增强,动物测试和部分临床疗效测试可能会逐渐减少,但临床药理学测试仍将是确保生物类似药质量的重要环节 。
由于生物类似药具有免疫原性,可能会引发一些安全问题,如患者免疫系统对其产生异常反应,导致治疗效果降低或需要停止治疗 。此外,生物类似药的分子结构较大且复杂,难以准确判断其与原研生物药是否完全平行,目前的分析方法虽然有了很大进展,但仍存在一定的局限性,不同实验室之间的数据比较也存在标准化的难题 。
生物类似药和靶向治疗各有优劣,靶向治疗药物能够精准作用于癌细胞的特定化学物质和蛋白质,而生物类似药不仅可以治疗多种疾病,还能在必要时提供个性化治疗,减少副作用 。未来,随着技术的不断进步,生物类似药有望在更多疾病的治疗中发挥更大作用,尤其是在癌症治疗领域,有望为患者提供更有效、更经济的治疗选择 。同时,在药物研发和应用过程中,需要更加注重药物的安全性、有效性以及质量控制,以确保患者能够从中获得最大的益处 。