产品中心
技术交流

扫描二维码
CAR-T技术的发展与应用
文章来源公众号:细胞基因研究圈 作者:南开细胞工程
✦
✦
✦
摘要:CAR-T细胞疗法是近年来癌症治疗领域的一项重大突破,它通过基因工程改造T细胞使其表达特异性靶向肿瘤抗原的嵌合抗原受体(CAR),从而高效清除肿瘤细胞。本文综述了CAR-T技术从基础研发到临床转化的演进历程,着重阐述在血液肿瘤、实体瘤、自身免疫性疾病等方面的研究进展,并对CAR-T技术的研究现状进行了综述,展望了其未来的研究方向。
01
✦CAR-T技术的概念及发展
✦✦✦

CAR-T,全称为 Chimeric Antigen Receptor T-Cell Immunotherapy(嵌合抗原受体T细胞免疫疗法)。它是一种高度个性化的细胞免疫治疗方法,被誉为肿瘤治疗领域的一场革命。其中T细胞来源于患者自身(自体)或健康供体(异体),是人体免疫系统中的“主力军”,能够识别并杀死异常细胞。嵌合抗原受体(CAR)是一个通过基因工程手段人工设计、合成的蛋白质受体。它被“安装”在T细胞的表面,充当一个“导航头”和“激活开关”。简单来说,CAR-T技术的原理就是通过基因工程,给患者的T细胞装上一套“GPS导航系统(CAR)”,使其能精准识别并高效摧毁带有特定“标签”(抗原)的肿瘤细胞,见图一。
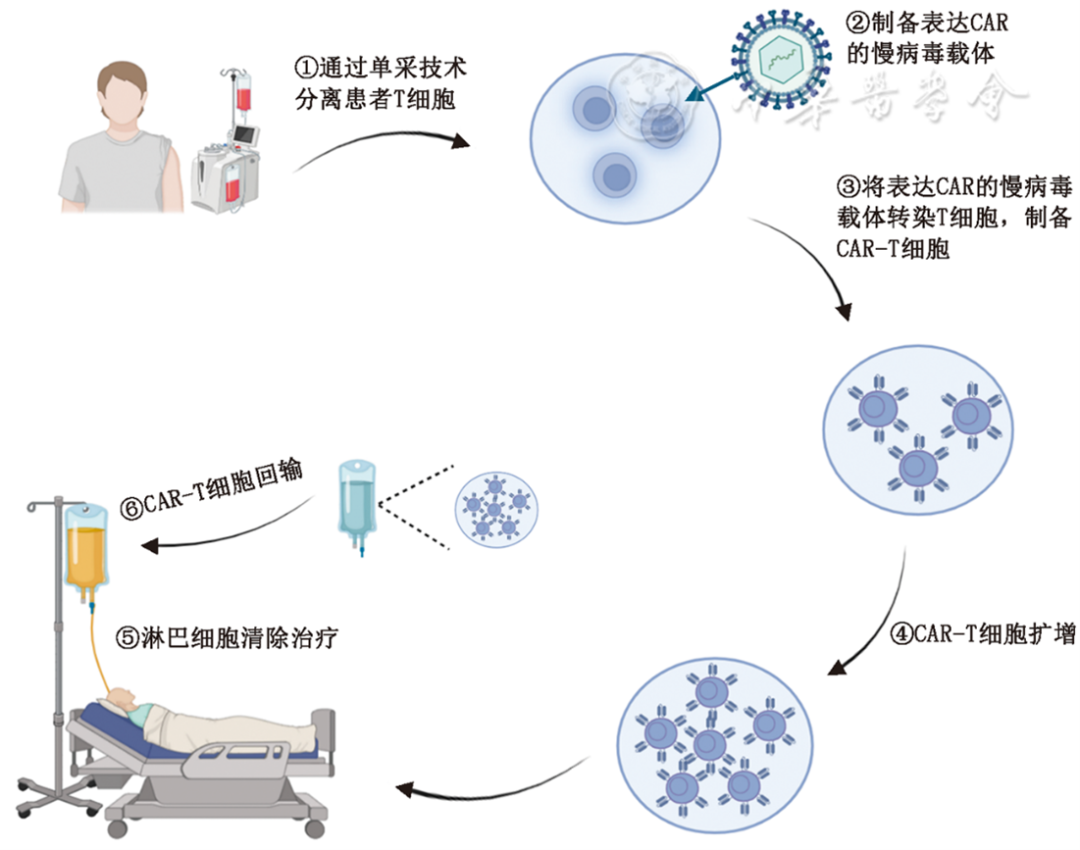
图1 CAR-T细胞治疗流程示意图[1]
然而CAR-T技术的发展并非一蹴而就,其历程大致可分为以下几个阶段:
1. 概念萌芽与初步探索
1987年首次提出了嵌合抗原受体(CAR)的概念;1989年首次将嵌合受体导入T细胞,实现了T细胞通过嵌合受体识别抗原。
2.技术突破与效果验证
其中共刺激信号的引入是CAR-T技术走向成功的最关键一步。研究人员(如Kowolik等研究人员)在CAR结构中加入了共刺激域(如CD28)[2]。这种改进如同给T细胞同时提供了“点火开关”和“加油踏板”,使其在体内的增殖、持久性和杀伤能力得到了指数级提升。
3. 临床转化与商业化
这一时期,大规模的临床试验不断证实了CAR-T在血液肿瘤中的巨大潜力。2017年成为CAR-T技术的“元年”。美国FDA首次批准了两款CAR-T产品上市:
Kymriah(诺华公司,靶向CD19):用于治疗儿童和年轻成人B细胞ALL。
Yescarta(Kite Pharma,靶向CD19):用于治疗特定类型的大B细胞淋巴瘤。
此后,多款靶向CD19或BCMA(用于多发性骨髓瘤)的CAR-T产品相继获批,标志着CAR-T疗法正式从实验室走向临床应用,成为一个全新的肿瘤治疗类别。
4. 深化发展与应对挑战
当前的研究重点在于解决CAR-T技术的局限性并拓展其边界:如应对实体瘤挑战、提升安全性与可及性、拓展适应症等。

✦
✦
✦
✦
✦
✦
02
✦CAR-T技术的应用
✦✦✦
1. 血液肿瘤
血液肿瘤主要分为白血病(Leukemia)、淋巴瘤(Lymphoma)和骨髓瘤(Myeloma)三大类。CAR-T细胞疗法作为血液肿瘤的主要治疗手段之一,也是第一个获得美国食品和药物管理局(FDA)批准用于临床的基因疗法,它通过调动患者自身的免疫系统来攻击癌细胞可有效医治复发/难治的B细胞淋巴瘤。有相关学者表示,治疗B细胞淋巴瘤的最佳选择是CAR-T,相较于其他的血液肿瘤治疗手段其对于复发和难治性患者的预后具有一定优势[3]。CAR-T细胞疗法为某些复发或难治性血液系统恶性肿瘤患者提供了新的治疗选择和治愈希望。虽然CAR-T技术目前主要集中在B细胞恶性肿瘤,且面临成本、毒副作用等挑战,但持续的科研创新和技术优化(如新型靶点、通用型CAR-T、联合策略等)正在不断推动这一领域向前发展,未来有望惠及更多患者。
✦
✦
✦
✦
✦
✦