产品中心
技术交流

扫描二维码
综述 | 通用型CAR免疫细胞临床研究进展及挑战
文章来源于微信公众号:中国肿瘤临床
摘要
通用型嵌合抗原受体T细胞(universal chimeric antigen receptor T-cell,UCAR-T)利用健康人群T细胞批量生产现货型嵌合抗原受体 T 细胞(chimeric antigen receptor T-cell,CAR-T)产品,解决了传统自体CAR-T成本高昂及制备周期过长的问题。目前,已有针对多个靶点的产品进入临床阶段,利用基因编辑技术有效降低了移植物抗宿主病(graft-versus-host disease,GvHD)风险。近年来,替代通用细胞来源(如NK细胞、NKT细胞、γδT细胞等)因其天然避免GvHD的特性而备受关注,为产品安全性提供了更大保障,同时基于不同细胞类型特性的个性化设计也为疗效提升带来了新的可能。本文对现有通用型嵌合抗原受体免疫细胞技术的主要临床研究进展、最新技术策略及面临的核心挑战进行系统概括,以期为寻找疗效和安全性间更优平衡,进一步拓宽其临床应用提供参考。
前言
自体嵌合抗原受体(chimeric antigen receptor,CAR)细胞治疗仍面临制备周期长、成本高昂、多线治疗后患者自身细胞状态不佳等问题,严重限制其临床应用[1]。相比之下,通用型嵌合抗原受体(universal chimeric antigen receptor,UCAR)免疫细胞通过对健康人群的免疫细胞进行改造,制备可长期储存、批量生产的“现货型”产品[2],在降低成本的同时也为疾病进展迅速的患者提供了治疗机会。尽管通用型CAR产品存在诸多优势,但仍面临显著挑战,包括免疫排斥等关键问题。特别值得注意的是,随着基因编辑技术的进步和新型细胞来源的探索,通用型CAR免疫细胞治疗正从血液肿瘤向实体瘤和自身免疫病领域快速拓展,本文将对最新临床进展进行系统梳理。
01 采用T细胞的临床研究进展
1.1 靶向CD19的通用嵌合抗原受体T细胞治疗 CD19自Pro-B阶段便开始持续表达,直至分化为浆细胞前,是嵌合抗原受体 T 细胞(chimeric antigen receptor T-cell,CAR-T)疗法中最早、最成熟的治疗靶点之一。美国Allogene Therapeutics公司的UCART19是全球首个进入临床试验的通用型CAR-T疗法,展现出较好的安全性和初步疗效,为UCAR-T技术的应用发展奠定了基础,见表1。该公司另一款面向复发难治性大 B 细胞淋巴瘤(relapsed/refractory large B-cell lymphoma,R/R LBCL)患者的Cema-Cel(前身为ALLO-501)产品最新发布的Ⅰ期数据(ALPHA NCT03939026,ALPHA 2 NCT04416984)显示,客观缓解率(objective response rate,ORR)和完全缓解率(complete response,CR)达到58%与42%,同时无移植物抗宿主病(graft-versus-host disease,GvHD)、≥3级细胞因子释放综合征(cytokine release syndrome,CRS)与免疫效应细胞相关神经毒性综合征(immune effector cell-associated neurotoxicity syndrome,ICANS)发生,展现出与自体CAR-T相当的安全性及疗效[3]。目前,该产品Ⅱ期ALPHA 3研究拟将Cema-Cel用于治疗在接受过6个周期利妥昔单抗、环磷酰胺、多柔比星、长春新碱联合泼尼松(R-CHOP)方案治疗或其他化学免疫疗法后仍存在微小残留病(minimal residual disease,MRD)阳性的患者,作为“第7个周期”的治疗方案,标志着向临床应用更进一步的发展。
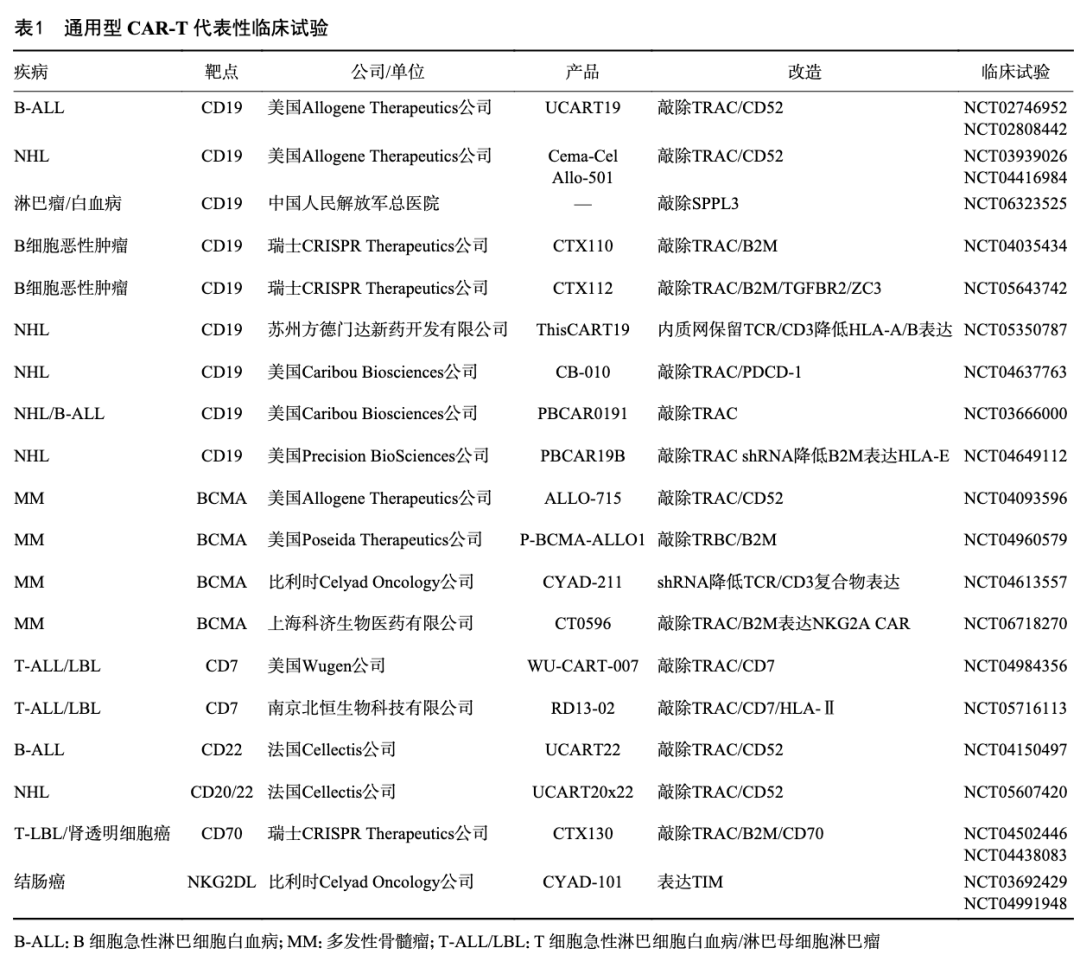
此外,最新研究表明,通过SPPL3基因编辑或LCK T316I突变联合Dasatinib等新型策略,可进一步延长UCAR-T细胞在患者体内的持久性。研究显示,靶向CD19的保留TCR通用型CAR-T在患者体内成功实现了长达6个月以上的持续存在,也为解决持久性难题提供了新思路[4-5]。 1.2 靶向BCMA的通用型CAR-T细胞治疗 多发性骨髓瘤(multiple myeloma,MM)是血液系统第二常见的恶性肿瘤,目前仍是不可治愈的疾病。ALLO-715 是首款靶向 BCMA 的UCAR-T 细胞产品,尽管与自体CAR-T相比在疗效上有所不足,但其安全性与有效性的验证仍为以BCMA为靶点的治疗带来了希望。与此同时,CT0596在Ⅰ期临床(NCT06718270)中初步展现出良好的安全性与应答率。在纳入的8例复发难治性多发性骨髓瘤(relapsed/refractory multiple myeloma,RRMM)/浆细胞白血病(plasma cell leukemia,PCL)患者中,5例达到部分缓解(partial response,PR)及以上疗效,包括3例完全缓解/严格意义的完全缓解(complete response/stringent complete response,CR/sCR)、1例非常好的部分缓解(very good partial response,VGPR)和1例PR,6例患者在第4周达到MRD阴性。安全性方面,患者仅观察到4例1级CRS,未见ICANS,整体耐受性良好。CT0596 在维持较高安全性的基础上展现出有希望的抗肿瘤潜力,为通用型 BCMA CAR-T 在多发性骨髓瘤中的进一步临床应用提供了重要证据[6]。 1.3 靶向CD7的通用型CAR-T细胞治疗 CD7在T细胞恶性肿瘤中高度表达,UCAR-T的特别优势在于其异体来源避免了T细胞被肿瘤污染。然而,靶向CD7的UCAR-T具有“自相残杀”现象,目前常采用基因编辑技术处理该问题,通过同时敲除CD7与TCR分子实现功能更强、安全性更高的CAR-T治疗。RD13-02敲除CD7、TRAC和HLA-Ⅱ相关基因,其一期临床试验(NCT05716113)结果显示,可评估的17例T细胞急性淋巴细胞白血病/淋巴母细胞淋巴瘤(T-cell acute lymphoblastic leukemia/lymphoblastic lymphoma,T-ALL/LBL)患者整体完全缓解/血液学恢复不完全的完全缓解(complete response/complete response with incomplete hematologic recovery,CR/CRi)率高达94%,在CR/CRi的患者中,100% 达到MRD阴性[7]。RD13-02在疗效上取得了十分显著的成绩,且≥3级不良反应均存在于相对高剂量组,剂量水平1(dose level 1,DL1)组展示了良好的耐受性。T细胞血液肿瘤复发后进展迅速,这使得通用型CAR-T的“即用性”优势尤为突出,为病情紧急的患者提供了及时的挽救措施,本临床试验数据也表明了UCAR-T技术有望大幅改善复发/难治性T-ALL/LBL患者的预后。 1.4 靶向其他靶点的通用型CAR-T细胞治疗 CD22可在CD19表达缺失的B细胞中维持表达,因此成为CD19的理想替代靶点。UCART22在Ⅰ期BALLI-01研究(NCT04150497)中展现出良好的安全性和初步疗效[8],验证了该靶点的可行性。Cellectis进一步推出双靶点产品UCART20x22(NCT05607420),提升了其抗肿瘤能力并降低抗原逃逸风险[9]。此外,CD70分子在多种血液系统肿瘤和实体瘤中存在异常表达[10]。CTX130的1期临床试验(NCT04502446)共纳入39例复发/难治性T细胞淋巴瘤患者,其中18例获得治疗反应[11],但CRS率达到67%,包括3例≥3级。目前,其下一代产品CTX131也已进入临床研发阶段,以期获得更好的安全性及疗效。 同时,通用型CAR-T在自身免疫病和实体瘤领域也取得了实质性进展。科济药业开发的靶向CD19/CD20的双靶点通用型CAR-T(KJ-C2219)已完成首例系统性红斑狼疮(systemic lupus erythematosus,SLE)患者的给药,证实了基于B细胞清除策略的通用型CAR-T在自身免疫性疾病中的临床可行性;CTX130在晚期肾透明细胞癌患者中也进行了临床试验(NCT04438083),81.3%的患者实现病情控制,其中1例患者获得持续3年的完全缓解,体现了其在实体瘤中的应用潜力[12]。
02 采用替代通用细胞的临床研究进展
2.1 NK细胞 NK细胞是先天免疫系统的重要组成部分,在天然规避GvHD风险的同时还可通过识别肿瘤细胞下调的MHC-Ⅰ分子和抗体依赖性细胞介导的细胞毒作用(antibody-dependent cell-mediated cytotoxicity,ADCC)来增强其杀伤能力,见表2。目前,已有众多不同来源的CAR-NK产品进入临床试验,除NK-92来源在疗效上有所不足,其余均展现出良好的安全性和一定的抗肿瘤效果,显示出值得期待的临床潜力。
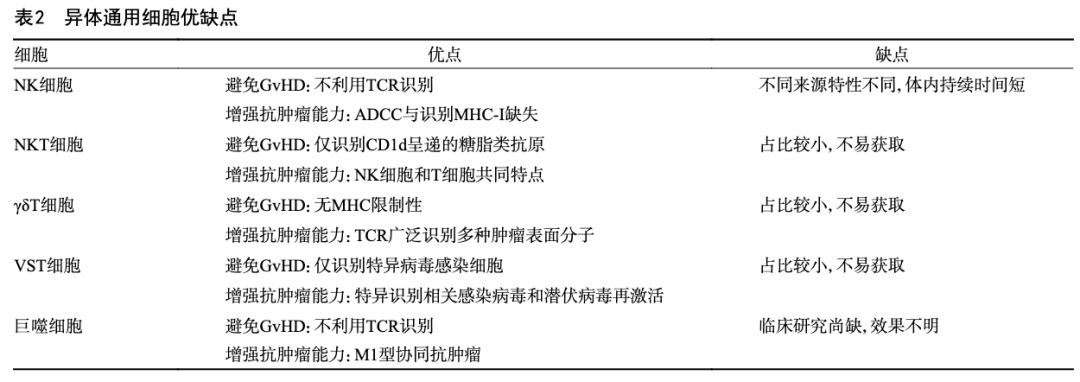
2.1.1 外周血和脐带血来源的CAR-NK 外周血NK拥有较强的抗肿瘤能力,但扩增能力有限;脐带血来源的NK细胞具有更强的增殖潜力,但细胞毒性相对较弱,需要通过特定的手段来进行激活。健康供体外周血来源的NKX019靶向CD19,其初步结果(NCT05020678)显示,在非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)患者中ORR达到71%,CR达到57%,但3例患者在至少6个月后复发;安全性上未见有剂量限制性毒性(dose-limiting toxicity,DLT)、ICANS、GvHD和≥3级CRS发生,见表3 [13]。
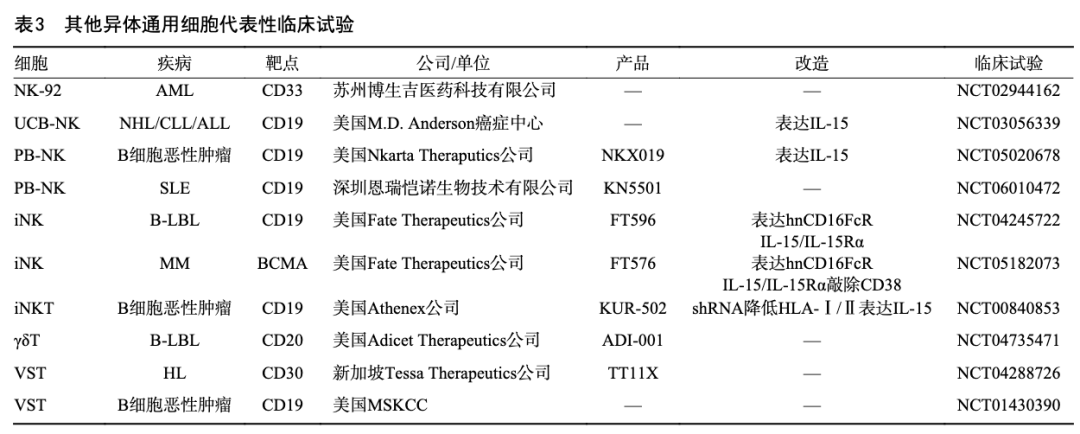
临床试验(NCT03056339)使用脐带血制造NK细胞,以CD19为靶点,面向R/R NHL、慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)及急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)患者[14]。在安全性方面,所有患者均未有≥3级CRS和ICANS、GvHD发生。在疗效上,D100时ORR和CR分别达到48.6%和29.7%,且CAR-NK细胞以低水平保持达12个月,验证了CAR-NK疗法的安全性与有效性。值得注意的是,通用型CAR-NK技术在自身免疫病领域也取得突破,恩瑞恺诺开发的靶向CD19的通用型CAR-NK(KN5501)已完成首例SLE患者的给药,标志着该技术正式从肿瘤领域拓展至自身免疫性疾病[15]。 2.1.2 iPSC来源的CAR-NK细胞 除上述提及的NK细胞来源外,诱导多能干细胞(induced pluripotent stem cells,iPSC)衍生的细胞也受到了广泛关注。iPSC来源可保证细胞有更好的一致性,并解决了细胞的来源不足问题,且易于进行CAR的插入。CAR-iNK产品FT596针对的是复发/难治性B细胞淋巴瘤患者,其Ⅰ期试验结果(NCT04245722)中联用利妥昔单抗组有20例患者曾接受过CAR-T治疗[16],其ORR达到45%,CR达到30%,显示出良好的初步疗效。FT596为CAR-T治疗失败的患者提供了一种新的挽救性治疗策略,凸显了CAR-iNK疗法的临床潜力。 2.2 NKT细胞 NKT细胞是一种具有NK细胞和T细胞特点的免疫细胞,特异性识别CD1d呈递的糖脂类抗原,不识别常规主要组织相容性复合体(major histocompatibility complex,MHC)复合物。KUR-502是同种异体的CAR-iNKT产品,其临床试验(NCT00840853)初步结果显示具有良好的耐受性,未报告GvHD,仅有1例1级CRS。同时,在7例NHL患者中,3例有治疗反应,其中2例达到CR。这项研究的初步结果表明了CAR-iNKT即使在低剂量下也能介导复发或难治性NHL患者的客观反应,验证了其治疗效果,也为以NKT为基础细胞的CAR技术做出了初步探索[17]。 2.3 γδT细胞 γδT细胞的TCR受体由γδ亚基组成,无MHC限制性,可直接识别多种肿瘤表面分子,成为另一种具有先天优势的细胞来源。一项靶向CD20的产品ADI-001目前已进入临床试验阶段(NCT04735471),其初步结果未报告≥3级CRS与ICANS,亦无GvHD发生。在疗效方面,ORR与CR均为78%,且曾接受过CD19 CAR-T治疗的4例患者达到100% CR,显示出对于CAR-T后复发患者良好的临床潜力[18]。但其在外周血的占比较低,在细胞的获取上有一定困难,从而限制了临床应用。 2.4 病毒特异性T细胞 病毒特异性T细胞(virus-specific T-cells,VST)是一种特异性识别并清除病毒感染的T细胞亚群,其TCR受到限制从而大幅降低了GvHD风险。一款EBV-VST来源的通用型CAR-T在临床试验中评估了其在复发/难治B细胞恶性肿瘤患者中用于移植后复发/移植后巩固治疗中多次输注的安全性(NCT01430390),1年和3年总生存(overall survival,OS)率为81%和75%;在接受治疗的16例患者中3例发生GvHD(1/2/3级各1例),未见≥3级CRS与ICANS。此外,与自体CAR-T相比,Tn、Tscm、Tcm比例较低,Tem与Te比例较高[19]。 2.5 巨噬细胞 巨噬细胞由于其趋化特性和抗肿瘤免疫能力,在实体瘤的治疗中展现出了新的可能,其不依赖TCR-MHC的识别,从而降低了GvHD的风险。同时其M1型也可以通过分泌细胞因子、招募肿瘤反应性T细胞和NK细胞等行为重塑肿瘤微环境,抑制M2型促肿瘤的存在,协同吞噬发挥抗肿瘤效果。异体CAR-M已在临床前试验中展示出了治疗潜力[20],但目前仍未有产品进入临床阶段。
03 通用型CAR免疫细胞疗法面对的主要挑战
尽管通用型CAR免疫细胞疗法展现出了较大潜力,但其临床应用仍面临着挑战,其中最主要的是移植物抗宿主病与宿主抗移植物反应(host-versus-graft,HvG)。因此,研究者提出了一系列应对策略,旨在进一步改善其安全性及疗效。 GvHD是利用外周血T细胞为来源的UCAR-T疗法中面对的关键问题之一。目前,避免GvHD最常用的手段为TCR受体的抑制,主要有基因编辑和非基因编辑两种方式(图1)。基因编辑方式主要通过破坏TRAC基因来消除TCR的表达,如CTX110。而非基因编辑技术目前主要包括质粒转入TIM分子从而竞争性抑制TCR识别,如CYAD-101;短发夹RNA(short hairpin RNA,shRNA)技术降低TCR复合物的表达,如CYAD-211;以及内质网保留技术,如ThisCART19等。相较于基因编辑存在潜在的脱靶风险,非基因编辑技术有着更好的安全性,有望成为未来通用型CAR-T疗法发展的重要方向。
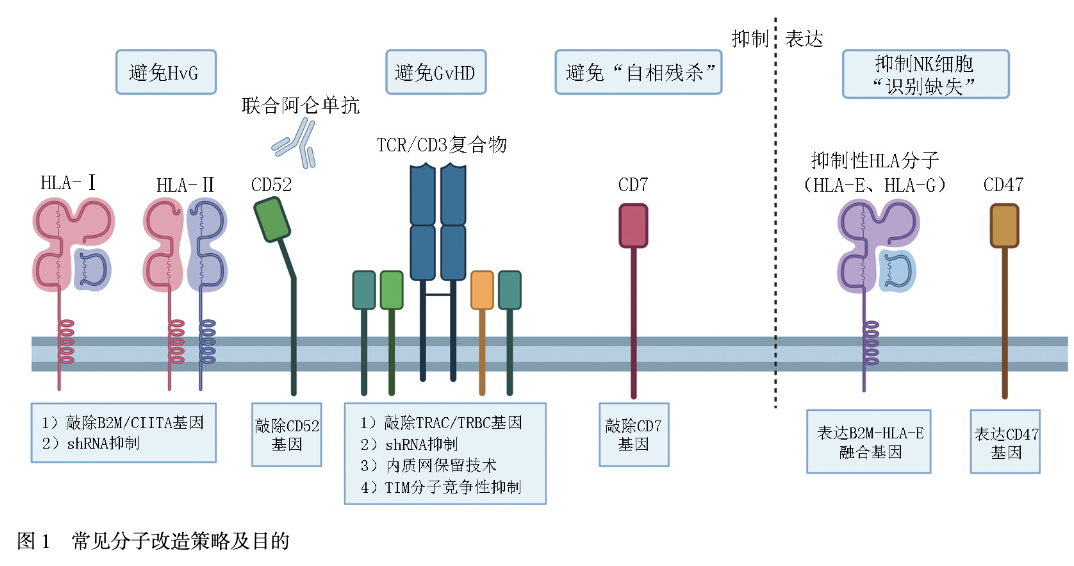
HvG是面临的另一项重要挑战。加强输注前的清淋是一种有价值的方法,目前常采用氟达拉滨+环磷酰胺(FC)方案联合阿仑单抗进行预处理,阿仑单抗可以结合宿主淋巴细胞表面存在的CD52,同时对CAR-T细胞进行CD52敲除,从而达到靶向清除的目的。虽然采用加强的化疗方案也可以深度清除淋巴细胞,但显著的骨髓抑制等也增加了患者的治疗风险。此外,改变MHC分子的表达也是一种有效的方法。许多临床试验采用基因编辑/非基因编辑技术敲除编码MHC-Ⅰ分子β2-微球蛋白的B2M基因,但MHC-I分子的缺失会导致NK细胞“自我缺失”效应。目前,已发现提高其他NK细胞抑制性分子(如HLA-E)的表达可以帮助解决这一问题[21]。而对于MHC-Ⅱ类分子,通常采用的方法是对其进行抑制,从而避免被CD4+T细胞识别杀伤。除了传统的基因编辑策略外,最新研究还探索了SPPL3基因编辑[4]、LCK T316I突变联合Dasatinib用药[5]等新型方案,在延长细胞持久性的同时保持更好的安全性特征。 由于通用型CAR-T大量利用基因编辑技术,其脱靶效应也值得关注。碱基编辑、表观遗传编辑等新型基因编辑技术通过避免DNA双链断裂,进一步改善了UCAR-T产品的安全性谱[22-23]。此外,通用细胞的批量制备使得环境中代谢产物积累增加,营养物质储存降低,最终影响产品质量,而进行代谢调控也可以增强细胞疗效[24]。同时,作为现货型治疗产品,细胞的冻存复苏也会对细胞状态产生影响,最终降低产品的效果[25]。
04 结语与展望
通用型CAR免疫细胞治疗技术由于其在成本、制作周期和可及性等方面的优势,已成为细胞免疫治疗的研究热点之一。传统T细胞利用新型基因编辑策略规避GvHD风险并延长持久性,目前已开展了许多针对不同靶点的临床试验,为复发难治患者提供了新的治疗手段;替代通用细胞无需基因编辑天然避免GvHD,也显示出了良好的安全性和一定的疗效,并且在自身免疫性疾病等领域展现出拓展潜力。UCAR-T技术仍面临着挑战,其中最核心的问题是免疫排斥,包括GvHD和宿主抗移植物反应,随着SPPL3编辑、碱基编辑等新技术的应用,上述问题正逐步得到解决。 总体而言,通用型CAR免疫细胞疗法具有广阔的应用前景,不仅在血液肿瘤领域,在实体瘤和自身免疫病方面也取得了一定的突破。未来研究方向应着重于优化通用细胞在体内的持久性并通过新型技术策略进一步降低免疫排斥的发生概率,在疗效和安全性之间寻找一个更优的平衡。随着技术的不断进步,通用型CAR免疫细胞技术有望扩展更广泛的适用范围,为更多患者带来希望。