产品中心
技术交流

扫描二维码
提高病毒载体滴度和质量研究:渗透压检测大显身手

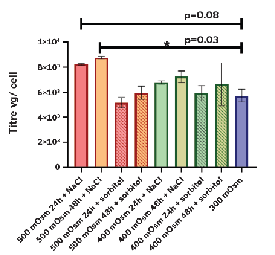
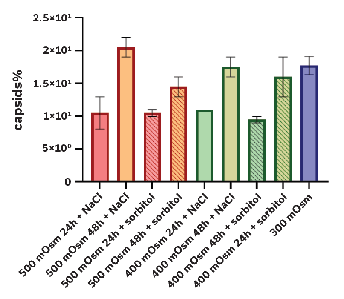
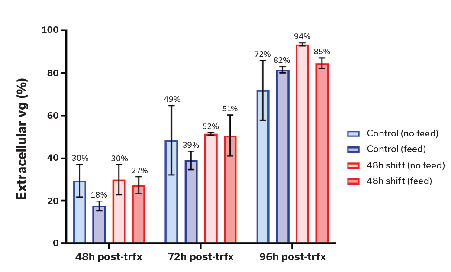
病毒载体的使用现在是细胞和基因治疗领域的一种常见方法,但在生产和工艺放大过程中存在诸多困难,其中三个主要痛点是:产率低(仅5-30%),质量差,以及整个工艺过程的效率。那么,在细胞和基因治疗领域改进的关键是什么?是实施高质量的工艺设计,包括工艺参数,以确保工艺流程中所有点的稳健性、可靠性和再现性。 渗透压是溶质浓度的量度,在整个细胞和基因治疗工艺中有许多应用。已有明确的证据表明,对这个关键过程参数的调控可以改善总体结果。为了进一步评估调控和优化渗透压对病毒载体的生产和工艺流程的影响,Advanced Instruments(安达望)和Cell and Gene Therapy Catapult进行合作研究,特别是针对AAV病毒载体,本次研究选择血清型AAV1为模型。 小规模培养对离子和非离子试剂进行筛选,以确定其中一种试剂是否对滴度有更大的实质性影响。与对照组(渗透压为300mOsm)相比,细胞感染后48h加入氯化钠将渗透压调整至500mOsm的培养条件下,特异性AAV滴度显著提高了25%(图1)。而产品质量与对照组相比,获得了更高的全/空壳率(如图2)。这一个结果为进一步改善上游工艺中AAV的产率和质量打开了大门。 图1 细胞感染后不同时间点通过氯化钠和山梨醇调整培养基渗透压对比对滴度的影响。 图2 不同时间点加入氯化钠和山梨醇的AAV全/空壳比例。 虽然渗透压优化具有提高滴度和质量的潜力,但由于高渗休克,导致细胞活力下降。为了解决这一问题,尝试在转染后6小时添加补料,维持细胞完整性、减少聚集并促进AAV的产生。对照组包含补料和不补料的两组培养,实验组分别设置补料和不补料培养策略下在细胞感染后48h时间点采用氯化钠将渗透压调整至500mOsm。 转染后72h到96h的总滴度没有变化,但细胞内外滴度比动态变化(图3)。在这里我们可以注意到渗透压的影响似乎是基质依赖性的,在转染后48小时,渗透压调整后的一小时内,补料的条件仅显示细胞外AAV比率增加。未补料的条件下,转染后96h细胞外AAV比率达到94%。 图3 在补料/无补料培养过程中,不同时间点的渗透压调整对细胞外病毒基因组比例的影响。 由于培养基的渗透压变化,从细胞外获得大部分产物,氯化钠的使用是一种低成本且可放大的解决方案,且在理想情况下可以除去细胞裂解步骤,从而消除了该步骤中产生的杂质。所有这些都可能帮助获得更好的产率,且对下游纯化产生深远的影响 在不同细胞培养策略下,在固定时间点改变渗透压,能够提高腺相关病毒1 (AAV)的总产量和产品质量,并且渗透压的调控还影响了胞内和胞外病毒载体的相对滴度,导致上清中胞外病毒颗粒的释放显著增加。这些发现对上游工艺和下游工艺都有潜在的深远影响,渗透压显然是优化病毒载体生产和工艺过程的关键。 尽管这项研究是以AAV1为模型进行研究的,但进行进一步的研究,并进行类似的试验,能够拓展应用到其他病毒载体的生产研究中。因此,将渗透压纳入不同生物工艺以改善痛点和瓶颈的前景是非常积极的,不仅上游过程,而且下游过程都有可能改变游戏规则。 生物制药生产涉及许多复杂的操作步骤,确保整个生产过程始终如一地生产符合预期产量、纯度和质量地生物制药产品。渗透压测试是工艺控制和质量控制的基本参数。OsmoTECH PRO渗透压仪是一种精准且易于使用地仪器,其拥有的先进数据管理选项得到了增强,可以无缝集成到高通量工作流程中。 历 史 推 荐 Cell and Gene Therapy Catapult成立于2012年,是一家通过弥合科学研究和产品全面商业化之间的差距来推动英国细胞和基因治疗行业发展的独立科研机构。该机构专注于细胞和基因治疗技术,与学术界和生物制药生产制造商保持着紧密的合作关系。同时该机构还拥有先进的科学技术和全方位的科研能力,帮助生物制药公司研发的产品顺利进入临床试验阶段。 长按或扫描上方二维码关注我们 Advanced Instruments成立于1955年,总部位于美国马萨诸塞州诺伍德,60 多年来一直致力于帮助生物制药,临床及食品饮料行业客户提升测试结果的质量,实现可信赖的实验结果,并不断提高企业的生产效率。 安达望(上海)科技有限公司是Advanced Instruments在中国依法成立的全资子公司。