产品中心
技术交流

扫描二维码
一个双特异性抗体的关键十年?
原创:泰有财 文章来源:抗体圈

介绍
自单克隆抗体被发现以来,可以作为治疗药物使用的双特异性版本就引起了极大的兴趣。然而,由于在临床试验中生成和生产双特异性抗体(bsAbs)以及对更复杂的机制(MOAs)的生物学理解方面的挑战,开发进程被放缓了。第一个bsAb,即EpCAM/CD3ε T细胞引导剂卡妥珠单抗,最终在2009年被批准用于治疗恶性腹水患者(图1)。这种bsAb随后在2013年从市场上撤回,可能与其只能腹腔内给药有关,因为当通过静脉给药时,患者会出现严重的输注反应,以及由于其大鼠-小鼠嵌合四价设计的完全功能性Fc部分导致的高免疫原性。从2009年到2020年,只有另外两种bsAbs被批准:(1) 2014年,无Fc串联单链可变片段(scFv)基础的CD19/CD3ε双特异性T细胞引导剂(BiTE)贝林妥单抗(Amgen)用于治疗急性淋巴细胞性白血病(ALL),和(2) 2017年,人源化异二聚体凝血因子IXa/X双特异性ART-Ig艾美珠单抗(Roche group),作为凝血因子VIII模拟物用于治疗血友病A(图1)。
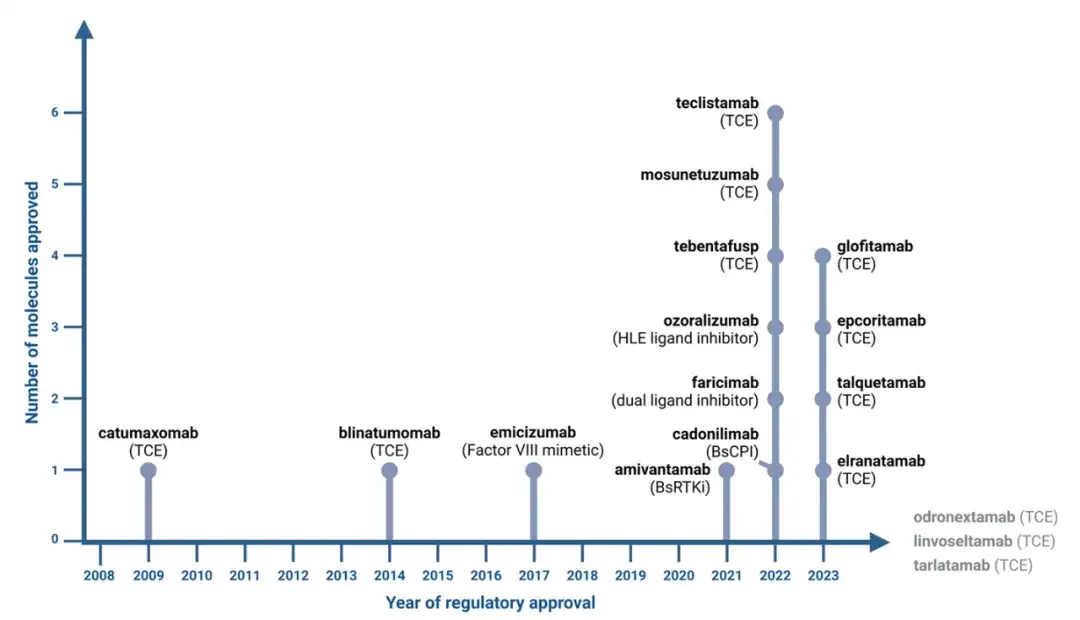
图1. 双特异性抗体监管批准的时间线及其相应的作用机制(MOA)。
Linvoseltamab、odronextamab和tarlatamab目前正在进行监管审查,预计2024年将有决定。使用http://Biorender.com创建。
由于对这些分子的极大兴趣以及在过去二十年中用于开发它们的技术的进展,已经描述、设计并临床前开发了数百种bsAbs。其中,超过100种bsAbs已经进入临床试验。基于在开发新型bsAb格式、新颖的靶标组合和双特异性领先分子方面的重大努力,最近的情况已经发生了实质性的变化,自2021年以来bsAb的批准变得频繁。仅在过去三年(2021-2023年),就有11种新的bsAb被美国、欧洲、日本和/或中国的卫生当局批准用于患者(图1,表1)。在这些11种bsAbs中,有九种被批准用于治疗癌症:(1) EGFR/c-MET bsAb amivantamab(强生公司(J&J))用于治疗带有EGFR外显子20插入突变的非小细胞肺癌(NSCLC),(2) gp100-pMHC/CD3ε bsAb tebentafusp(Immunocore)用于治疗无法切除或转移性葡萄膜黑色素瘤,(3) CD20/CD3ε T细胞引导剂(TCE) mosunetuzumab(Roche group)用于治疗复发/难治性(R/R)滤泡性淋巴瘤,(4) PD-1/CTLA-4 bsAb cadonilimab(Akeso)用于治疗复发或转移性宫颈癌患者,(5) BCMA/CD3ε TCE teclistamab(J&J)用于治疗R/R多发性骨髓瘤,(6) CD20/CD3ε TCE glofitamab(Roche group)用于治疗R/R弥漫性大B细胞淋巴瘤(DLBCL),(7) CD20/CD3ε TCE epcoritamab(AbbVie/Genmab)用于治疗R/R DLBCL,(8) GPRC5D/CD3ε TCE talquetamab(J&J)用于治疗R/R多发性骨髓瘤和(9) BCMA/CD3ε TCE elranatamab(辉瑞)用于治疗R/R多发性骨髓瘤。
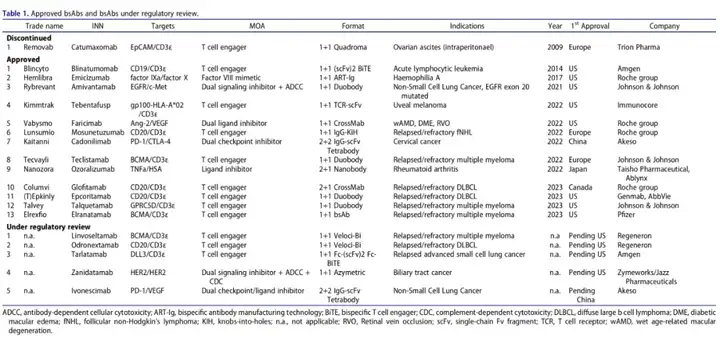
两种额外的双特异性抗体(bsAbs)被批准用于非肿瘤适应症,针对VEGF-A/Ang-2的双特异性抗体faricimab(罗氏集团)用于治疗湿性年龄相关性黄斑变性、糖尿病性黄斑水肿和视网膜静脉阻塞后的黄斑水肿,这是首个被批准用于眼科的双特异性抗体,以及针对TNF/人血清白蛋白(HSA)的双特异性抗体ozoralizumab(大正制药)用于治疗难以控制的类风湿性关节炎。罗氏集团与中外制药目前以四种获批的双特异性抗体领先该领域,紧随其后的是强生公司,拥有三种获批的双特异性抗体。值得注意的是,在目前获批的13种双特异性抗体中,有两种,emicizumab和faricimab,已经实现了重磅炸弹的地位,年销售额分别超过四十亿和二十亿美元,突显了这种新型治疗类药物的商业前景。
双特异性抗体格式
开发的双特异性抗体格式的多样性反映了在这些获批的双特异性抗体中应用的技术多样性(图2)。各自的双特异性抗体格式涵盖了非IgG样的双特异性抗体,包括1)安进公司的短半衰期串联scFv基础的BiTE格式,应用于blinatumomab,2)Immunocore公司的T细胞受体(TCR)-scFv融合基础的ImmTac格式,应用于tebentafusp,以及3)Ablynx公司的三价双特异性串联纳米抗体格式,通过HSA结合延长半衰期,应用于ozoralizumab。然而,大多数双特异性抗体是IgG样分子,其药代动力学与抗体相似,因为存在Fc。五种非对称1+1 IgG样双特异性抗体源自于控制的Fab臂交换,基于Duobody技术,应用于amivantamab、talquetamab、辉瑞公司的teclistamab、epcoritamab,或者相关链交换技术,应用于elranatamab。或者,通过中外制药的ART-Ig技术强制正确的链关联,应用于非对称1+1 IgG样双特异性抗体emicizumab以及常见的轻链。正确的重链关联也可以通过应用在mosunetuzumab中的knobs-into-holes技术来确保,或者与CrossMab技术一起应用,以强制正确的轻链关联在1+1 IgG样双特异性抗体faricimab中。最后,Akeso的cadonilimab包含一个对称的四价2+2 C末端IgG-scFv融合。在获批的双特异性抗体中,有四种应用了Genmab的Duobody技术,三种应用了基因泰克的knobs-into-holes技术,以及两种应用了罗氏pRED的CrossMab技术。可用格式的多样性表明“标准化”的双特异性抗体不太可能出现,但近期的批准强调了对经典异源二聚体IgG样双特异性抗体格式的关注。这些双特异性抗体通常显示出IgG样的药代动力学和低发生率的抗药物抗体。
获批双特异性抗体的作用机制
TCE是双特异性抗体,一个特异性结合到细胞表面肿瘤抗原,另一个特异性结合到TCR复合体的一个亚单位,因此在同时结合到肿瘤抗原和TCR时,T细胞随后被激活以杀死肿瘤细胞,分泌细胞因子并开始增殖。显然,T细胞的参与严格依赖于双特异性,并且不能通过两种传统单克隆抗体的组合来实现。在癌症治疗中,占主导地位的作用机制是T细胞的参与,获批和临床试验中最多的双特异性抗体是TCE。图2a显示了获批TCE双特异性抗体格式的演变。这类分子包括用于治疗复发/难治性血液癌症的TCE:1)CD19/CD3ε blinatumomab用于治疗ALL,2)CD20/CD3ε TCE mosunetuzumab用于治疗R/R非霍奇金淋巴瘤(NHL),以及glofitamab和epcoritamab用于治疗R/R DLBCL,3)BCMA/CD3ε TCE teclistamab、elranatamab和GPRC5D/CD3ε talquetamab用于治疗R/R多发性骨髓瘤。虽然通常T细胞参与治疗实体瘤似乎更具挑战性,可溶性的gp100-肽MHC/CD3ε特异性TCR-scFv融合tebentafusp是首个被批准用于治疗葡萄膜黑色素瘤的TCE,为在血液肿瘤之外的使用提供了证据。
血友病A是一种遗传性出血性疾病,其特征是缺乏血液凝固因子VIII。虽然可以给患者注射重组因子VIII,但这与因子VIII生产、短半衰期频繁给药和中和抗体的发展等挑战有关。为此,中外制药设计并优化了IXa/X双特异性抗体emicizumab,使其通过将酶因子IXa和底物因子X拉近,模仿血液凝固因子VIII的功能,同时展现出延长的药代动力学。
单特异性受体酪氨酸激酶阻断单克隆抗体,如抗EGFR的cetuximab和panitumumab或抗HER2的trastuzumab和pertuzumab,已经彻底改变了癌症治疗。尽管在靶向额外RTKs方面进展甚微,但针对两个RTKs同时的EGFR/c-Met双特异性抗体amivantamab最近被批准用于治疗具有EGFR外显子20插入突变的特定亚组NSCLC患者。除了其双重信号抑制功能,包括通过阻断配体结合位点和通过受体下调,amivantamab还包含一个afucosylated Fc部分,以介导增强的抗体依赖性细胞毒性(ADCC)以促进NK细胞和巨噬细胞/单核细胞的参与。
在过去的十年中,获批的免疫检查点抑制性抗体,包括针对PD-1(nivolumab、pembrolizumab、cemiplimab)、PD-L1(atezolizumab、avelumab、durvalumab)和CTLA-4(ipilimumab、tremelimumab)的抗体,已经彻底改变了癌症治疗领域,并确立了癌症免疫疗法。基于这一经验,设计了双重PD-1/CTLA-4检查点抑制性双特异性抗体cadonilimab,目标是专门且理想地同时结合并抑制抗原特异性T细胞上的PD-1和CTLA-4,以克服检查点抑制。
促血管生成因子VEGF-A和Ang-2通过促进视网膜血管生成和破坏血管稳定性,导致渗漏、随后的水肿和炎症,从而促成视力丧失。VEGF-A和Ang-2在眼睛中干扰血管生成、稳定血管并减少渗漏和炎症(图2e)。为了最小化外周活动并消除FcγR的结合,它被设计为带有工程化的Fc部分,具有Triple A FcRn和P329G LALA突变,以实现FcRn循环。
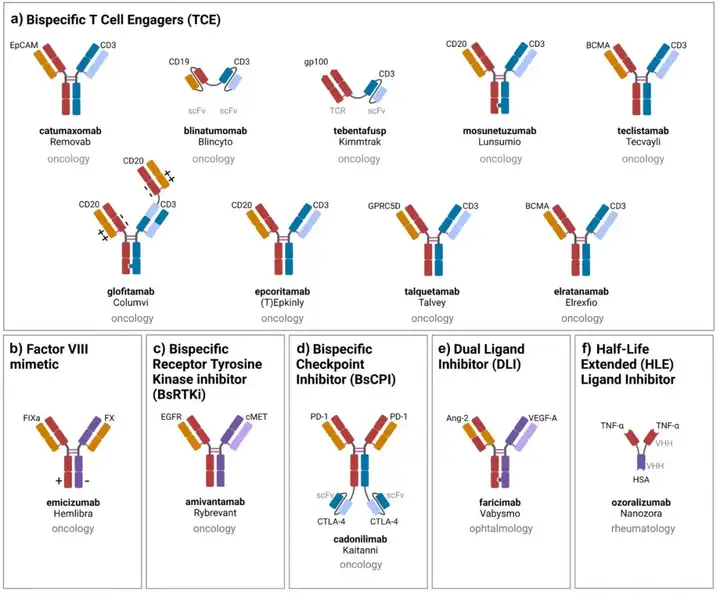
图2. 获批双特异性抗体(bsAbs)的示意图、适应症和作用机制:a) T细胞引导剂(TCE),b) 因子VIII模拟物,双重信号抑制:c) 双特异性受体酪氨酸激酶(RTK)抑制剂(BsRtki),d) 双特异性检查点抑制剂(BsCPI),e) 双配体抑制剂(DLI),f) 半衰期延长(HLE)配体抑制剂。使用http://Biorender.com创建。
值得注意的是,双特异性是考虑眼内给药时的一个主要优势。对于TNF配体抑制剂ozoralizumab,应该指出,从功能上讲,这种纳米抗体结构像一个单特异性抗体一样阻断TNF,第二个单一域特异性仅需要通过与HSA结合来实现IgG样的药代动力学,而不依赖于Fc部分,从而实现FcRn循环。
在增强内源性或预先存在的免疫反应的研究领域,另一个主要的研究领域仍然是开发针对例如PD-1和CTLA-4或LAG-3(tebotelimab)的双重靶向检查点抑制性双特异性抗体。这些双重检查点抑制剂中有几个目前正在进行高级临床试验,结果将显示它们在疗效和/或安全性方面是否优于相应的PD-1/PD-L1单克隆抗体与CTLA-4或LAG-3单克隆抗体的组合。值得注意的是,双重靶向PD-1/VEGF抑制性双特异性抗体ivonescimab目前正在中国国家药品监督管理局进行监管审查,用于治疗NSCLC。
展望未来
在这十年中,已经有11种双特异性抗体获得批准,预计未来几年将有更多的具有改变医疗实践潜力的双特异性抗体获得批准。在肿瘤学领域,开发差异化的双重RTK信号抑制剂,并通过双特异性抗体共靶向不同的细胞表面受体,仍然是一个活跃且先进的临床研究领域。一些例子包括:EGFR/LGR5如petosemitab,HER3如zenocutuzumab,HER2或双伞型双特异性抗体靶向HER2如zanidatamab,目前正在美国进行审查。
鉴于双特异性抗体的多功能性和介导完全新颖的作用机制的潜力,双特异性抗体领域有望看到新出现的方法和候选药物进入临床试验,希望在未来几年内,在肿瘤学和非肿瘤学适应症中,包括感染/病毒学、自身免疫、代谢、神经学和眼科等领域,提供关键数据。这些新概念包括最近描述的不同方法,包括:1)与TCE不同的效应细胞引导者,如髓系细胞、NK或γδ-T细胞,2)原位组装概念,以特别激活在双重靶标表达细胞上的双特异性抗体或在肿瘤微环境中,3)PROTAC类方法导致膜蛋白的内化和降解,4)基于抗体的细胞因子模拟物触发细胞因子受体,以及5)独特的解决方案,用于传递双特异性抗体超越障碍,如血脑屏障,包括双伞型单特异性双特异性抗体靶向HER2如zanidatamab zovodotin(ZW49)或c-MET与REGN5093。
开发用于治疗不同血液恶性肿瘤的TCE将继续是合成免疫方法领域的一个主要研究领域,因为这类治疗已经证明了其益处。到目前为止,基于Regeneron的VelociBi技术的不对称1+1 TCE odronextamab(CD20/CD3ε)和linvoseltamab(BCMA/CD3ε)目前正在进行监管审查,可能会在2024年获得批准,还有各种其他的TCE正在进行高级临床开发,用于NHL、多发性骨髓瘤和AML。重要的是,新出现的数据显示,TCE将来也可能在实体瘤中找到更广泛的应用。事实上,最近已经发布了针对Amgen的1+1 DLL3/CD3ε Fc-BiTE tarlatamab治疗R/R小细胞肺癌的有希望的临床数据,目前正在进行监管审查,以及Xencor/Amgen的2+1 STEAP1/CD3ε XmAb xaluritamig用于治疗R/R前列腺癌。这些数据支持了这样一个观点,即足够肿瘤特异性以实现强大的抗肿瘤效果,同时限制靶标外肿瘤毒性的实体瘤靶标是可用的。在这种情况下,像蛋白酶激活这样的肿瘤激活机制旨在增加针对实体瘤的TCE的治疗窗口。
基于TCE的作用机制,为T细胞提供TCR信号1,目前正在快速临床采用靶向CD28或4-1BB/CD137的共刺激双特异性抗体,为T细胞提供信号2,从而实现持续和更持久的T细胞反应,这可能对治疗神经退行性疾病和其他疾病有应用。
【关于逐典】
上海逐典生物科技有限公司,坐落于中国(上海)自由贸易试验区,获得ISO9001质量体系认证,是一家从事重组蛋白研发和销售的高新科技企业。
逐典生物始终秉持以客户为中心的理念,针对重组蛋白的结构设计、纯化工艺及其稳定剂型相关的多项关键技术进行优化。专业定向蛋白变复性技术,可将大肠杆菌大量表达的变性固体蛋白转变成高活性可溶性蛋白。凭借技术优势,逐典生物新品研发周期短且可控性强,为重组蛋白的高质高效研发提供保障,为企业生产降本增效。
公司自成立以来成功开发百余种高活性细胞因子及多种高活性蛋白酶,覆盖细胞培养、病毒纯化以及质量分析等生物工艺各个环节。可广泛应用于科研、医药生产及IVD(体外诊断试剂)等领域,满足各类用户所需。
