产品中心
技术交流

扫描二维码
利用结合Fc片段结合的纳米抗体做偶联药物
文章来源公众号:Drugs and technology 作者:福尼亚吹风
澳大利亚蒙纳士大学药物科学研究所Angus P. R. Johnston教授团队在Nature Nanotechnology期刊在线发表题为“A versatile antibody capture system drives specific in vivo delivery of mRNA-loaded lipid nanoparticles”的研究论文。该研究报道了一种针对IgG Fc片段结合的纳米抗体TP1107,可将抗体以最优取向固定在脂质纳米颗粒(LNPs)表面,无需对抗体进行修饰或复杂纯化。
开发一种简单、高效的方法,将抗体以最佳取向固定在LNP表面,实现mRNA的细胞特异性递送,避免传统抗体修饰方法导致的取向随机、亲和力下降、工艺复杂等问题。
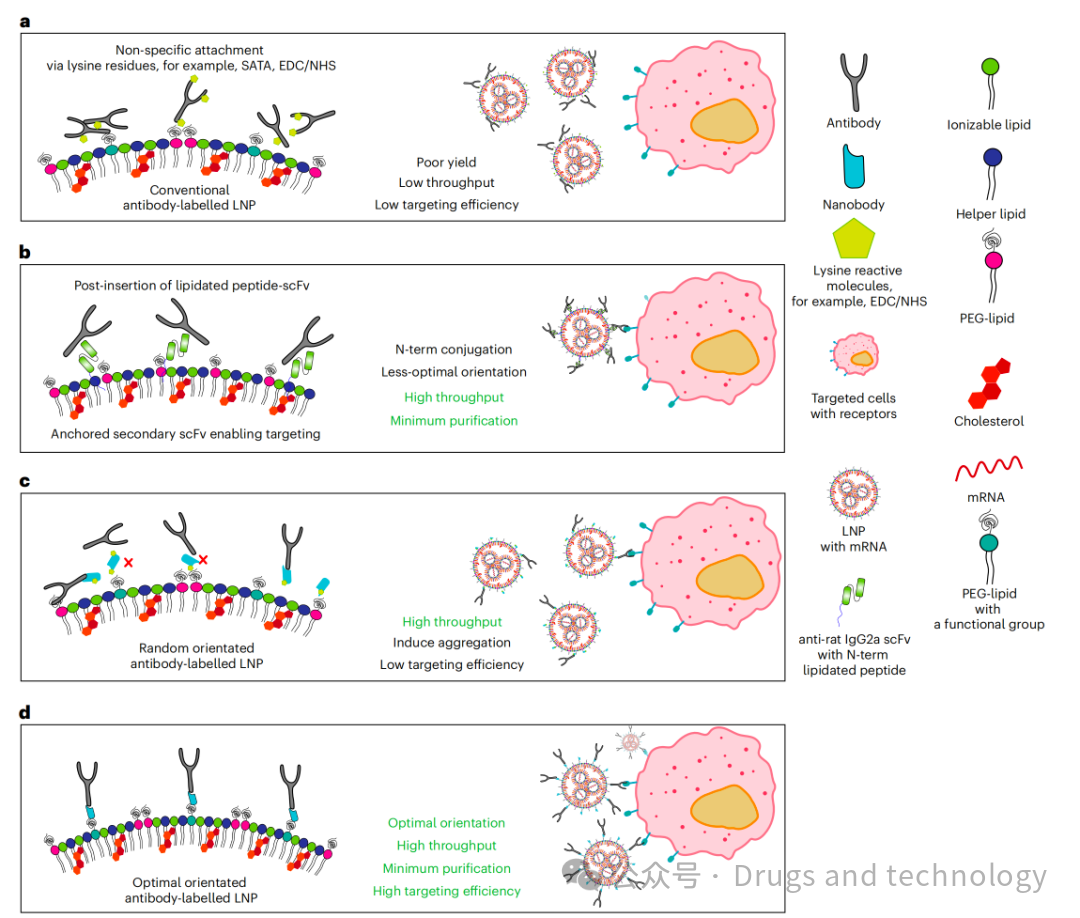
下图a. 示意图比较传统抗体偶联方法。通常,抗体通过琥珀酰亚胺酯与天然存在的赖氨酸残基随机反应的方式与纳米颗粒偶联,这会导致抗体在纳米颗粒表面取向随机,从而损害其活性。
b. ASSET技术:脂化scFv的后插入。使用经过N端脂化肽修饰的工程化抗大鼠IgG2a单链可变片段(scFv),可将抗体捕获在LNP表面。
c. 通过NHS-叠氮化物与赖氨酸残基偶联的抗小鼠/抗大鼠IgG1纳米抗体TP1107允许高通量评估抗体;然而,抗体仍然是随机取向的。
d. 最优取向TP1107以最佳取向捕获抗体,最大限度地提高了结合效率,并能够实现简单快速的抗体筛选。
核心技术:TP1107纳米抗体捕获系统
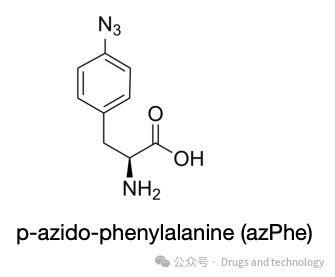
原理:使用一种名为 TP1107 的抗Fc纳米抗体,通过位点特异性修饰(在Gini5位点引入叠氮苯丙氨酸azPhe),使其以最优方向结合小鼠IgG1的Fc段。
优势:无需抗体修饰:只需将抗体与TP1107功能化的LNPs混合即可捕获。
最佳取向:确保抗体抗原结合域朝向外部,最大化靶向效率。
无需纯化:高亲和力结合,捕获效率高,省去后续纯化步骤。
结构解析:通过冷冻电镜确定TP1107与IgG1的结合位点,指导最优连接位点选择。
纳米抗体修饰:
TP1107optimal:位点特异性引入azPhe,与DBCO-PEG-DSPE通过点击化学反应连接。
TP1107random:通过NHS-azide随机修饰赖氨酸,模拟传统方法。
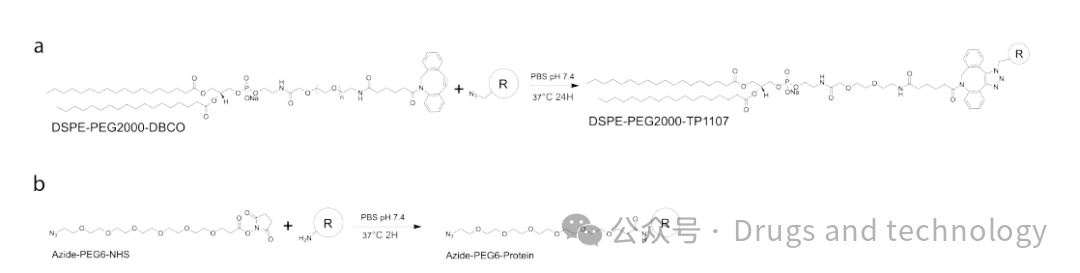
LNP功能化:将脂质化的TP1107插入预形成的LNPs中,再捕获目标抗体。
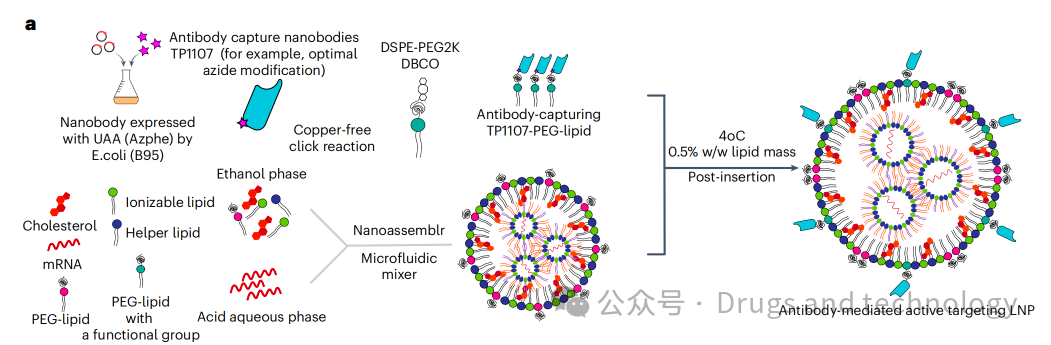
📊 主要实验结果
1. 靶向效率显著提升
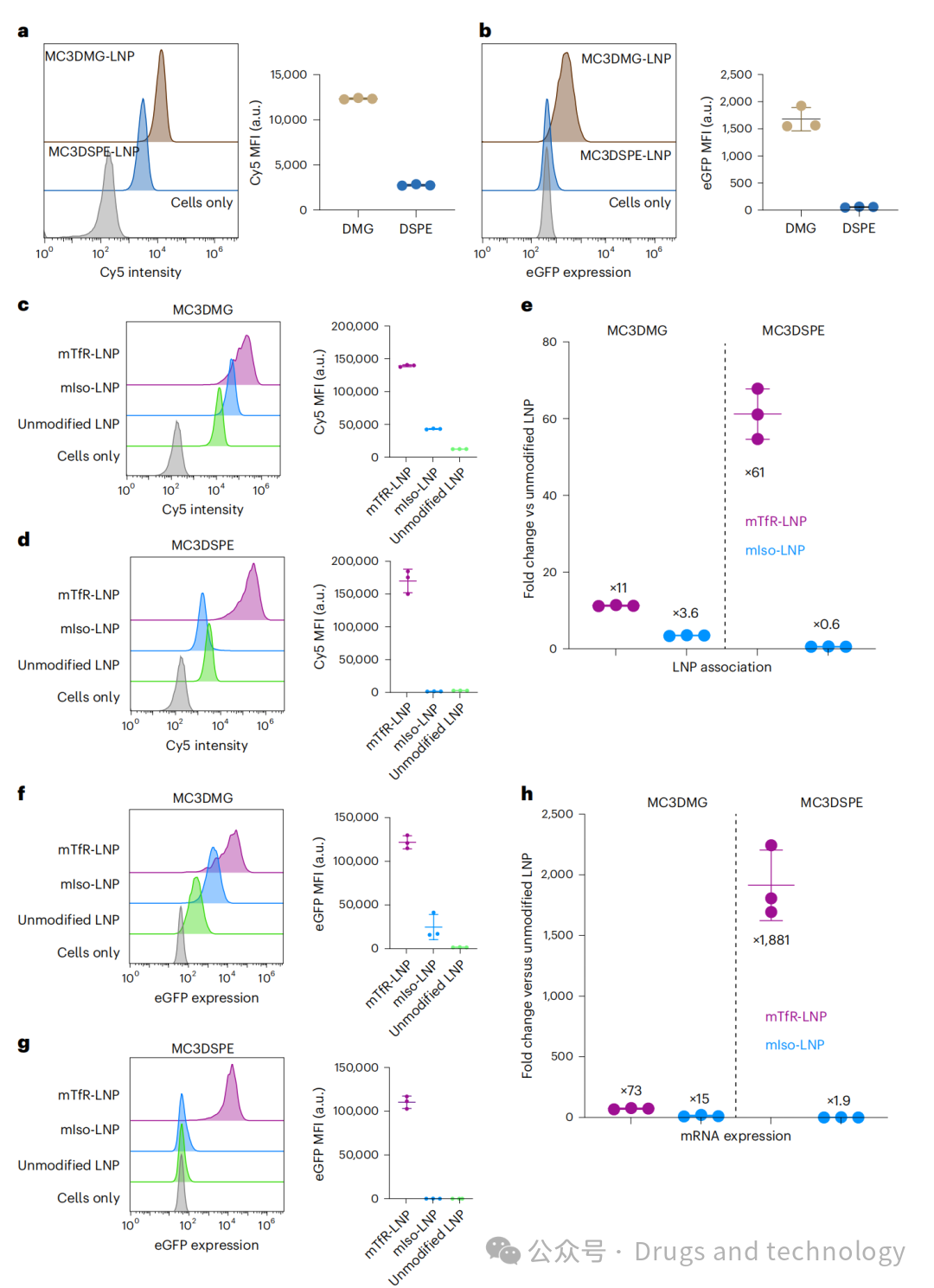
与未靶向LNPs相比,mRNA表达量提升超过1000倍。
与传统随机抗体偶联方法相比,表达量提升超过8倍。
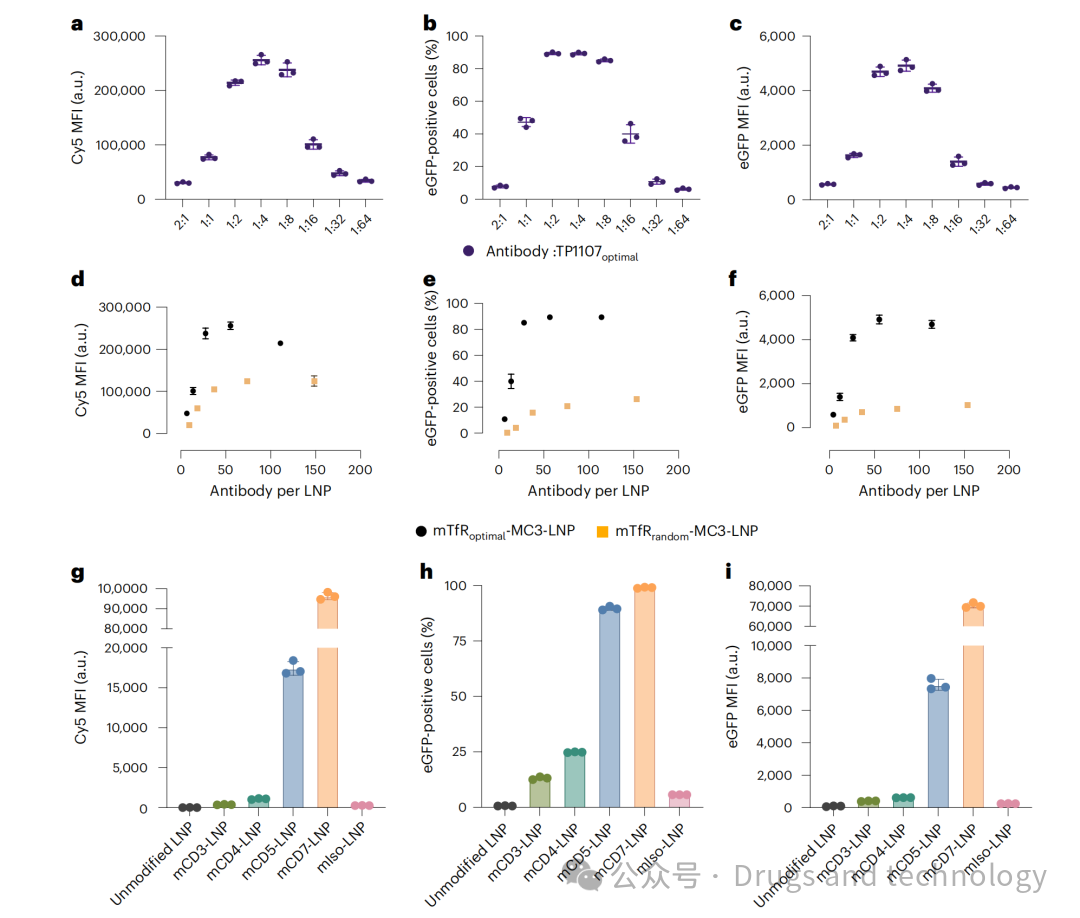
2. 细胞特异性强
在Jurkat细胞和原代人PBMCs中,CD3/CD5/CD7靶向LNPs能高效转染T细胞,几乎无脱靶表达。
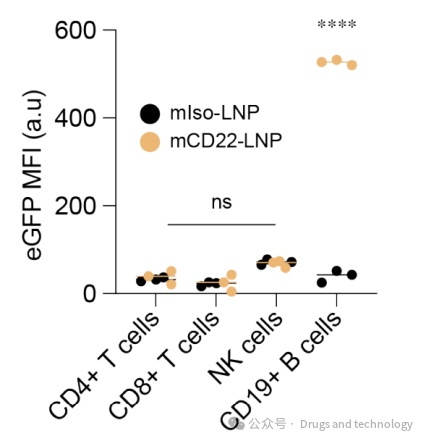
CD22靶向LNPs可特异性转染B细胞,展示平台的多功能性。
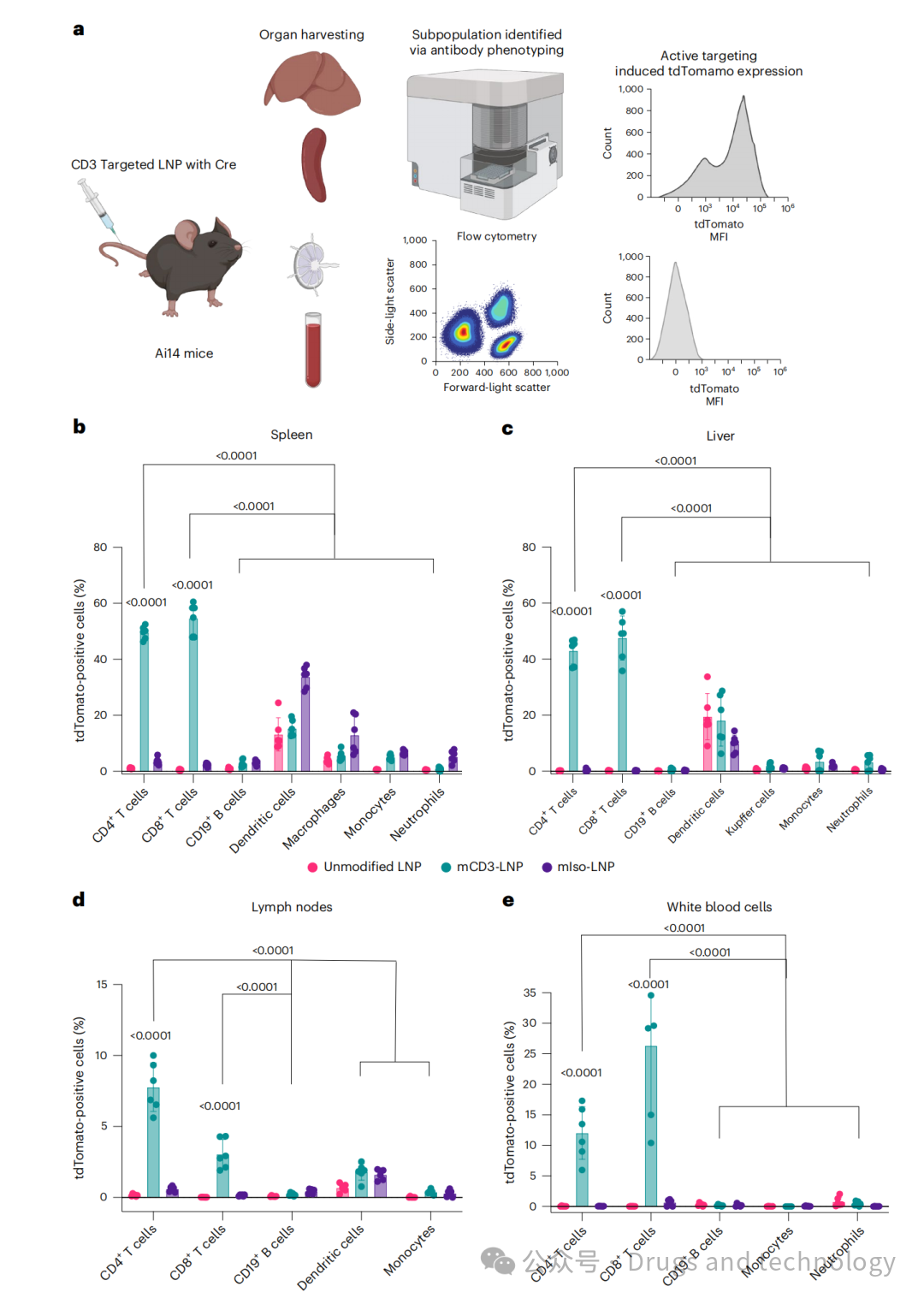
3. 体内靶向验证
在Ai14报告小鼠中,CD3靶向LNPs能高效、特异性地将Cre mRNA递送给T细胞(脾脏、肝脏、淋巴结、血液中均有显著tdTomato表达),且几乎不靶向其他免疫细胞。
4. 安全性良好
未引起显著体重下降或肝毒性。
本研究开发了一种简便、高效、可扩展的抗体捕获平台,无需抗体修饰即可实现最优取向的功能化,显著提高LNP的靶向效率与mRNA表达。
该平台可快速筛选不同抗体,推动mRNA疗法向非疫苗领域(如免疫调控、细胞重编程)转化。
精确的体内T细胞靶向及良好的安全性为临床转化奠定基础,未来可拓展至其他核酸药物与细胞类型。